题目内容
课本中有一问:为什么汗水有咸味?某校学习小组同学为此开展探究.
【提出问题】汗水中产生咸味的物质是什么?
【假设与猜想】根据生活经验推测,汗水中产生咸味的物质可能是 .
【查阅资料】用铂丝醮取少许含有钠元素的溶液(或物质)在酒精灯火焰上灼烧,会呈现黄金火焰.
【制订计划】为了证明咸味物质是猜想中的物质,一是要证明汗水溶液中含有阴离子 (填写离子符号).二是要证明汗水溶液中有阳离子 (填写离子符号).
【进行实验】证明阴离子的实验,向汗水溶液中滴加 溶液,再加入少量稀硝酸,振荡,仍有白色沉淀产生.
证明阳离子的实验: .
【结论】经上述实验证明,汗水中的咸味物质就是猜想中的物质.
【分析与交流】上述实验中,证明阴离子存在的化学反应方程式为: ,该反应属于 .
【提出问题】汗水中产生咸味的物质是什么?
【假设与猜想】根据生活经验推测,汗水中产生咸味的物质可能是
【查阅资料】用铂丝醮取少许含有钠元素的溶液(或物质)在酒精灯火焰上灼烧,会呈现黄金火焰.
【制订计划】为了证明咸味物质是猜想中的物质,一是要证明汗水溶液中含有阴离子
【进行实验】证明阴离子的实验,向汗水溶液中滴加
证明阳离子的实验:
【结论】经上述实验证明,汗水中的咸味物质就是猜想中的物质.
【分析与交流】上述实验中,证明阴离子存在的化学反应方程式为:
考点:实验探究物质的组成成分以及含量,常见离子的检验方法及现象,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【假设与猜想】
根据生活经验推测,氯化钠有咸味,汗水中产生咸味的物质可能是氯化钠;
【制订计划】
为了证明咸味物质是氯化钠,一是要证明汗水溶液中含有阴氯离子,二是要证明汗水溶液中有钠离子;
氯离子能和银离子结合成不溶于稀硝酸的白色沉淀--氯化银;
氯化钠溶液中的钠离子在灼烧时能够产生黄色火焰;
【分析与交流】
氯化钠能和硝酸银反应生成白色沉淀--氯化银和硝酸钠,根据反应物、生成物的种类可以判断反应类型.
根据生活经验推测,氯化钠有咸味,汗水中产生咸味的物质可能是氯化钠;
【制订计划】
为了证明咸味物质是氯化钠,一是要证明汗水溶液中含有阴氯离子,二是要证明汗水溶液中有钠离子;
氯离子能和银离子结合成不溶于稀硝酸的白色沉淀--氯化银;
氯化钠溶液中的钠离子在灼烧时能够产生黄色火焰;
【分析与交流】
氯化钠能和硝酸银反应生成白色沉淀--氯化银和硝酸钠,根据反应物、生成物的种类可以判断反应类型.
解答:解:【假设与猜想】
根据生活经验推测,汗水中产生咸味的物质可能是氯化钠.
故填:氯化钠.
【制订计划】
为了证明咸味物质是猜想中的物质,一是要证明汗水溶液中含有阴离子--氯离子,二是要证明汗水溶液中有阳离子--钠离子;
进行实验:证明阴离子的实验,向汗水溶液中滴加硝酸银溶液,再加入少量稀硝酸,振荡,仍有白色沉淀产生;
证明阳离子的实验:用铂丝醮取少许汗水,在酒精灯火焰上灼烧,呈现黄色火焰.
故填:Cl-;Na+;硝酸银;用铂丝醮取少许汗水,在酒精灯火焰上灼烧,呈现黄色火焰.
【分析与交流】
氯化钠和硝酸银反应的化学方程式为:NaCl+AgNO3═AgCl↓+NaNO3,氯化钠和硝酸银相互交换成分,生成氯化银和硝酸钠,属于复分解反应.
故填:NaCl+AgNO3═AgCl↓+NaNO3;复分解反应.
根据生活经验推测,汗水中产生咸味的物质可能是氯化钠.
故填:氯化钠.
【制订计划】
为了证明咸味物质是猜想中的物质,一是要证明汗水溶液中含有阴离子--氯离子,二是要证明汗水溶液中有阳离子--钠离子;
进行实验:证明阴离子的实验,向汗水溶液中滴加硝酸银溶液,再加入少量稀硝酸,振荡,仍有白色沉淀产生;
证明阳离子的实验:用铂丝醮取少许汗水,在酒精灯火焰上灼烧,呈现黄色火焰.
故填:Cl-;Na+;硝酸银;用铂丝醮取少许汗水,在酒精灯火焰上灼烧,呈现黄色火焰.
【分析与交流】
氯化钠和硝酸银反应的化学方程式为:NaCl+AgNO3═AgCl↓+NaNO3,氯化钠和硝酸银相互交换成分,生成氯化银和硝酸钠,属于复分解反应.
故填:NaCl+AgNO3═AgCl↓+NaNO3;复分解反应.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
下列物质中属于混合物的是( )
| A、冰水混合物 | B、纯净的空气 |
| C、氧气 | D、二氧化碳 |
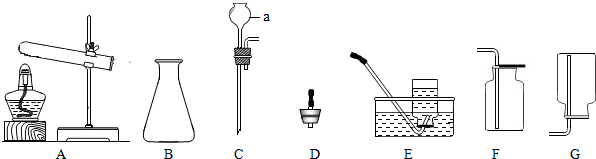
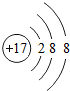 用下面给定的四种粒子的符号或示意图,完成下列问题(用符号或化学式填空,多个答案必须全部填写):
用下面给定的四种粒子的符号或示意图,完成下列问题(用符号或化学式填空,多个答案必须全部填写):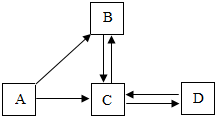 A、B、C、D四种物质含有相同的一种元素,其中A是一种固体单质,D不溶于水,B、C的组成元素相同,它们之间的转化关系如图所示.
A、B、C、D四种物质含有相同的一种元素,其中A是一种固体单质,D不溶于水,B、C的组成元素相同,它们之间的转化关系如图所示.