题目内容
【题目】图中①、②为氧元素、铝元素在元素周期表中的信息示意图,A、B、C、D是四种粒子的结构示意图,根据图示回答下列问题:
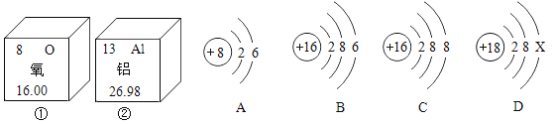
(1)氧元素属于_____元素(填“金属”或“非金属”),若一个铝原子的相对原子质量是27,则这个铝原子的中子数是_____。
(2)C粒子的符号为_____,若D为原子,则X=_____。
(3)A、B、C、D中属于同种元素的是_____(填序号)。
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似_____(填序号)。
【答案】非金属 14 S2﹣ 8 BC B
【解析】
(1)氧元素属于非金属元素;相对原子质量≈质子数+中子数,单位不是g,若一个铝原子的相对原子质量是27,则这个铝原子的中子数是:27﹣13=14。
(2)原子中,核电荷数=核内质子数=核外电子数=原子序数;核内质子数<核外电子数时,该粒子为阴离子;C粒子是带2个单位负电荷的硫离子,可以表示为S2﹣;若D为原子,则X=18﹣2﹣8=8。
(3)A、B、C、D中属于同种元素的是BC,这是因为它们的核内质子数相等。
(4)A粒子的化学性质与B粒子的化学性质相似,这是因为它们的最外层电子数相等。

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
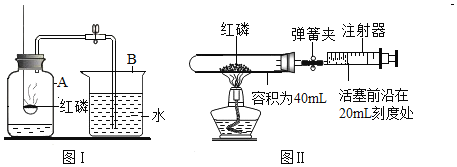
名牌中学课时作业系列答案【题目】某研究小组用下图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。
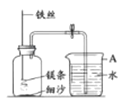
实验前,小组成员提出了不同的猜想。
【猜想与假设】
猜想1:可以代替,因为镁条与氧气反应后不会产生气体
猜想2:不能代替,查阅资料知金属镁很活泼,可能会与空气中的氮气反应
【进行实验】
步骤 | 实验操作 | 实验现象 |
Ⅰ | 组装好装置后,打开止水夹,手捂集气瓶,一段时间后,松开手 | 烧杯中导管口有气泡冒出,松手后,烧杯中导管末端有一段液柱 |
Ⅱ | 关闭止水夹,点燃镁条,迅速伸入集气瓶中,塞好塞子 | 镁条燃烧,放出大量热,发出耀眼白光,生成大量白烟,剩余固体为白色带状物 |
Ⅲ | 冷却至室温,打开止水夹 | 烧杯中水从导管进入集气瓶中,体积约为集气瓶体积的2/5 |
【解释与结论】
(1)Mg与氧气反应的化学方程式为_________。
(2)步骤Ⅰ说明装置的气密性_________。
(3)步骤Ⅱ中,关闭止水夹的目的是_________。
(4)推测猜想2成立的现象证据是_________。
【反思与评价】
(5)该小组认为,即使步骤Ⅲ中水的体积恰好占集气瓶体积的1/5,也不能说明猜想1成立,理由是_________。
(6)小组中同学对镁条与瓶中气体的反应提出了进一步的猜想:甲同学认为镁条先与O2反应,乙同学认为镁条先与N2反应。为进一步检验他们的猜想,可以进行的实验操作是:取少量镁条,点燃后迅速放入盛有空气的集气瓶中,待镁条熄灭后,________。
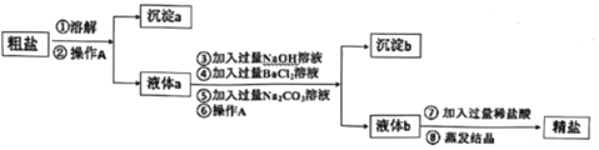
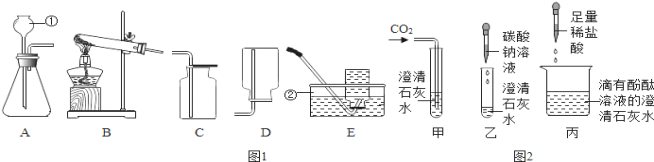
【题目】石家庄28中化学兴趣小组的同学在学习九年级《化学》下册中的资料卡片“石笋和钟乳石的形成”时,发现难溶于水的碳酸钙当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:CaCO3+CO2+H2O=Ca(HCO3)2,联想到实验室中澄清石灰水与二氧化碳反应会生成碳酸钙:Ca(OH)2+CO2=CaCO3↓+H2O,对长时间向碱溶液中通入CO2反应后溶液中的溶质组成产生了浓厚的兴趣。
(提出问题)一定量CO2与NaOH溶液反应后的溶质组成是什么?
(查阅资料)(1)通入少量CO2反应的化学方程式为:___。
(2)通入过量CO2,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3。
(3)碳酸氢盐都是可溶于水的,BaCO3难溶于水。
(4)碳酸氢钠溶液呈碱性。
(提出猜想)(1)溶质为NaOH和Na2CO3; (2)溶质为Na2CO3;(3)溶质为___(填化学式);(4)溶质为NaHCO3。
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
(1)用玻璃棒蘸取反应后溶液,滴在pH试纸上 | pH=9 | 该溶液显碱性 |
(2)取反应后溶液少许于试管中,向其中滴加过 量的___溶液 | 有___生成 | 猜想(4)不成立 |
(3)取步骤(2)中的上层清液,滴入稀盐酸 | 有气泡冒出 | 猜想(1)和(2) 不成立 |
(得出结论)猜想(3)成立。
(讨论交流)(1)有同学提出,实验步骤(1)是多余的,你认为该实验设计是否需要,___(填“需要”或“不需要”)。
(2)同学们又一次把目光投向了教材,发现遇热或压强变小时:Ca(HCO3)2=CaCO3↓+CO2↑+H2O,纷纷提出,干粉灭火器中用NaHCO3灭火的反应原理与之相似,试写出NaHCO3受热分解的化学方程式:__。
(反思应用)同学们回忆起实验室检验二氧化碳的情景,心想:如果向澄清石灰水中不断通入二氧化碳,会看到怎样的现象呢?请你描述一下:___。