题目内容
【题目】根据如图所示实验,并阅读小资料,回答下列问题。

![]() 小资料
小资料
二氧化硫与氢氧化钠溶液反应,生成亚硫酸钠,亚硫酸钠溶于水,二氧化硫与水反应生成亚硫酸,亚硫酸是液体。
(1)图1中反应的文字表达式为___________,现象为____________,集气瓶中加入水的作用是___________。
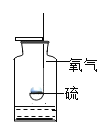
(2)图2中反应的文字表达式为____________,集气瓶中加入的液体可能是_____________,其目的为__________。
【答案】铁+氧气![]() 四氧化三铁 剧烈燃烧、火星四射、放出大量的热、生成黑色固体 防止燃烧生成的高温熔融物溅落炸裂瓶底 硫+氧气
四氧化三铁 剧烈燃烧、火星四射、放出大量的热、生成黑色固体 防止燃烧生成的高温熔融物溅落炸裂瓶底 硫+氧气![]() 二氧化硫 氢氧化钠溶液 吸收二氧化硫,防止污染空气(合理即可)
二氧化硫 氢氧化钠溶液 吸收二氧化硫,防止污染空气(合理即可)
【解析】
铁在氧气中点燃生成四氧化三铁,硫在氧气中点燃生成二氧化硫,二氧化硫与氢氧化钠溶液反应,生成亚硫酸钠。
(1)图1中反应是铁在氧气中点燃生成四氧化三铁,反应的文字表达式为铁+氧气![]() 四氧化三铁,现象为剧烈燃烧、火星四射、放出大量的热、生成黑色固体,集气瓶中加入水的作用是防止燃烧生成的高温熔融物溅落炸裂瓶底。
四氧化三铁,现象为剧烈燃烧、火星四射、放出大量的热、生成黑色固体,集气瓶中加入水的作用是防止燃烧生成的高温熔融物溅落炸裂瓶底。
(2)图2中反应是硫在氧气中点燃生成二氧化硫,反应的文字表达式为硫+氧气![]() 二氧化硫,二氧化硫和氢氧化钠反应,集气瓶中加入的液体可能是氢氧化钠溶液,其目的为吸收二氧化硫,防止污染空气。
二氧化硫,二氧化硫和氢氧化钠反应,集气瓶中加入的液体可能是氢氧化钠溶液,其目的为吸收二氧化硫,防止污染空气。

 阅读快车系列答案
阅读快车系列答案【题目】根据下列装置,结合所学化学知识回答下列问题:
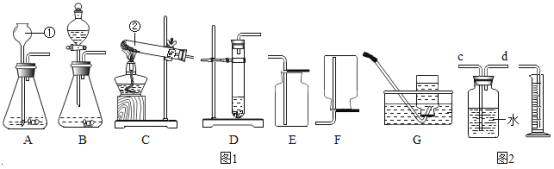
(1)写出图1中标号仪器的名称:①_______;②_____;
(2)实验室用双氧水和二氧化锰制取氧气时,收集装置选用_____,能用此收集方法的原因是_____,写出该反应的文字表达式_____,二氧化锰是该反应的_____.
(3)实验室用高锰酸钾制取氧气时,发生装置应选用_____(填字母);其反应的文字表达式_____,二氧化锰是该反应的_____.
(4)如用G装置收集氧气,开始收集的最佳时刻是_____,
(5)为了测量生成氧气的体积可用图2装置,氧气从_____端进入(填序号),量筒的作用是_____.
(6)小柯为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
收集方法 | 向上排空气法 | 排水法 | ||||
氧气浓度% | 79.6 | 79.7 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气平均浓度% | 79.7 | 89.7 | ||||
①小柯用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到_____________为氧气集满的标准。
②以上两种方法中, _______法收集到的氧气更纯净。
③向上排空气法收集到的氧气浓度只有80%左右的原因有(_________)
A 氧气的密度略大于空气的密度
B 加热高锰酸钾固体产生氧气的浓度只有80%左右
C 当观察到带火星木条复燃时,集气瓶内还有空气
D 当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
【题目】小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示的探究实验:
实验操作 | 实验现象 | 实验结论或总结 | ||
结论 | 总结 | |||
实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是_______________。 | 二氧化锰是过氧化氢分解的催化剂。 |
实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰和水混合不能产生氧气。 | |
实验三 | 向盛有5mL5%过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条 | ____________ | 二氧化锰能加快过氧化氢的分解。反应的文字表达式是______________。 | |
(1)请你帮小丽同学填写上表中未填完的空格。
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是______。
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”, 过氧化氢在常温下分解缓慢,加入二氧化锰反应明显加快,若要证明二氧化锰是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的________和_________是否改变。