题目内容
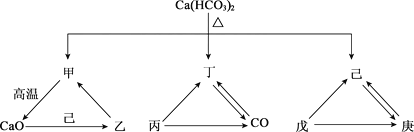
【题目】A~F是初中化学常见物质,A、B、C、D和CaCO3均含有同一种元素,其中B常用于改良酸性土壤,胃液中含有F。它们之间的转化关系如图所示,“→”表示相互转化。请回答:

(1)A的俗称是______。
(2)写出下列反应的化学方程式:
D→C______________________________;
B→CaCO3__________________________。
(3)从微观角度考虑,B和F反应的实质是_____和____结合生成水;该类反应我们常常称为______反应。
【答案】 生石灰 CaCl2+2AgNO3═Ca(NO3)2+2AgCl↓ CO2 +Ca(OH)2 ===CaCO3↓+H2O H+ OH﹣ 中和
【解析】B常用于改良酸性土壤,B是Ca(OH)2 ,胃液中含有HCl,故F是HCl,则D是CaCl2,A是CaO,C是Ca(NO3)2。(1)A是CaO,俗称是生石灰。(2)D→C反应的化学方程式为:CaCl2+2AgNO3==Ca(NO3)2+2AgCl↓,B→ CaCO3 的化学方程式为:
CO2 +Ca(OH)2 ===CaCO3↓+H2O (3)从微观角度考虑,酸碱反应的实质是 H+、 OH﹣结合生成水,酸碱之间的反应称为中和反应。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氮肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表。

反应前 | 反应后 | |
烧杯和样品溶液总质量 | 氯化钡溶液质量 | 过滤后烧杯和溶液总质量(滤液的损失忽略不计) |
45g | 55g | 76.7g |
反应的化学方程式为(NH4)2SO4+BaCl2═BaSO4↓+2NH4Cl,其他成分能溶于水但不参加反应。
(1)反应共生成BaSO4的质量为 g。
(2)若所取氮肥样品的质量为15g,试通过计算确定氮肥中硫酸铵的纯度是否与标签相符。(请写出计算过程)
(3)反应前后,溶液中硫元素的质量 (填“不变”、“增大”或“减小”)。其原因是 。