题目内容
小明同学在学习酸的性质时,他用大小,外形均相同的铝片分别和H+浓度相同的稀盐酸、稀硫酸反应.他意外地发现:铝片与稀盐酸反应放出气泡的速度明显快于与稀硫酸反应放出气泡的速度.是什么原因导致了反应现象的差异呢?小明从微观角度分析得出,H+浓度相同的盐酸、硫酸中,只是所含______不同.小明提出了以下猜想:①Cl-能促进铝和酸的反应,SO42-对反应无影响;
②Cl-对反应无影响,SO42-能抑制铝和酸的反应;
③Cl-能促进铝和酸的反应,SO42-能抑制铝和酸的反应;
他进行了如下实验探究:
| 组别 | 相同的铝片 | 浓度相同的酸 | 反应片刻后添加少量某种试剂 | 添加试剂后反应现象 | 结论 |
| 1 | 1g铝片 | 5mL盐酸 | Na2SO4 | 无明显变化 | ______离子对反应无影响 |
| 2 | 1g铝片 | 5mL盐酸 | NaCl | 明显加快 | ______离子对反应有促进作用 |
(1)请将表格中的空格补充完整;
(2)上述猜想______是成立的;
(3)若将第2组实验中添加的试剂NaCl改为HCl气体,能否完成探究任务?请说明原因.______.
【答案】分析:(1)中反应条件中铝片的大小、外形均相同,H+浓度相同的稀盐酸、稀硫酸反应,只有酸根离子不同.
(2)从第一组试验中后来只加入了Na+、SO42-对实验没有影响.Na+、SO42-对反应没影响.在第二组实验加入了Na+、Cl-,反应明显加快,综合可知Na+对实验没影响,所以影反应速率的是Cl-.
(3)HCl气体溶于水后变成了盐酸,增加了盐酸浓度,改变了实验条件,起不到对比实验的作用.
解答:解:反应条件中铝片的大小、外形均相同,H+浓度相同的稀盐酸、稀硫酸反应,只有酸根离子不同.
故答案为:酸根离子;
(1)第一组试验中加入了硫酸钠后反应速度无变化,则Na+、SO42-对实验没有影响.
故答案为:Na+、SO42-;Cl-
(2)根据上面结论可以得出Cl-能促进铝和酸的反应,SO42-对反应无影响.
故答案为:①
(3)HCl气体溶于水后变成了盐酸,增加了盐酸浓度,改变了实验条件,起不到对比实验的作用.
故答案为:不能,由于HCl气体溶于水生成盐酸,增加了溶液中氢离子浓度,实验条件发生了变化.
点评:本题在考查“影响反应速率的因素”这个知识点时,采用了多个不同的例子,通过对比实验,得到结果分析生成结论,注重考查学生的分析问题和解决问题的能力.
(2)从第一组试验中后来只加入了Na+、SO42-对实验没有影响.Na+、SO42-对反应没影响.在第二组实验加入了Na+、Cl-,反应明显加快,综合可知Na+对实验没影响,所以影反应速率的是Cl-.
(3)HCl气体溶于水后变成了盐酸,增加了盐酸浓度,改变了实验条件,起不到对比实验的作用.
解答:解:反应条件中铝片的大小、外形均相同,H+浓度相同的稀盐酸、稀硫酸反应,只有酸根离子不同.
故答案为:酸根离子;
(1)第一组试验中加入了硫酸钠后反应速度无变化,则Na+、SO42-对实验没有影响.
故答案为:Na+、SO42-;Cl-
(2)根据上面结论可以得出Cl-能促进铝和酸的反应,SO42-对反应无影响.
故答案为:①
(3)HCl气体溶于水后变成了盐酸,增加了盐酸浓度,改变了实验条件,起不到对比实验的作用.
故答案为:不能,由于HCl气体溶于水生成盐酸,增加了溶液中氢离子浓度,实验条件发生了变化.
点评:本题在考查“影响反应速率的因素”这个知识点时,采用了多个不同的例子,通过对比实验,得到结果分析生成结论,注重考查学生的分析问题和解决问题的能力.

练习册系列答案
相关题目
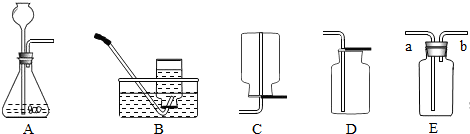
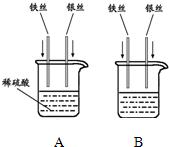
 16、通过实验探究的方法对未知事物进行探索是化学学习的一种重要学习方式.请回答下列有关问题:
16、通过实验探究的方法对未知事物进行探索是化学学习的一种重要学习方式.请回答下列有关问题: