题目内容
【题目】空气是宝贵的自然资源,下图是以空气等为原料合成尿素[CO(NH2)2]的流程。请按要求回答相关问题:
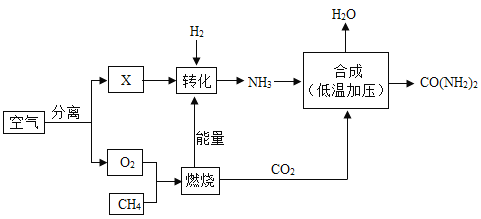
(1)空气属于____________填(“纯净物”或“混合物”),X 是空气中含量最多的气体,其化学式为_____________。
(2)图中分离空气的过程属于______变化(填“物理”或“化学”)。
(3)空气中含有的少量稀有气体的化学性质_____(填“活泼”或“稳定”)。
(4)实验室制取二氧化碳的化学反应方程式为_____;二氧化碳的密度比空气____________填“大”或“小”)。
(5)①天然气的主要成分是甲烷(化学式 CH4),甲烷中碳元素的质量分数为_______________。
②点燃 CH4 之前应_____。8 g CH4 完全燃烧消耗 32gO2,生成 a g CO2 和 18g H2O,则a= ________________________g。
(6)写出 NH3 合成尿素的化学反应方程式_____。
【答案】混合物 N2 物理 稳定 CaCO3+2HCl═CaCl2+H2O+CO2↑ 大 75% 检验其纯度 22 CO2+2NH3 CO(NH2)2+H2O
CO(NH2)2+H2O
【解析】
(1)空气中含有多种成分,属于混合物;X是空气中含量最多的气体,该气体是氮气,其分子式为N2,
故填:混合物;N2。
(2)图中分离空气的过程没有生成新物质,属于物理变化,
故填:物理。
(3)空气中含有的少量稀有气体的化学性质稳定,
故填:稳定。
(4)实验室用大理石和稀盐酸制取二氧化碳,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学反应方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳的密度比空气大,故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;大;
(5)①天然气的主要成分是甲烷(化学式 CH4),甲烷中碳元素的质量分数为:![]() =75%,故填:75%。
=75%,故填:75%。
②可燃性气体不纯时点燃或加热可能产生爆炸,故点燃CH4之前应检验甲烷的纯度。8gCH4完全燃烧消耗32gO2,生成agCO2和18gH2O,则a=8g+32g-18g=22g,故填:检验甲烷的纯度;22。
(6)尿素只含有营养元素氮元素,属于氮肥;二氧化碳和NH3在低温高压下能反应生成尿素和水,化学反应方程式为CO2+2NH3 CO(NH2)2+H2O.故填:氮肥;CO2+2NH3
CO(NH2)2+H2O.故填:氮肥;CO2+2NH3  CO(NH2)2+H2O。
CO(NH2)2+H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案