题目内容
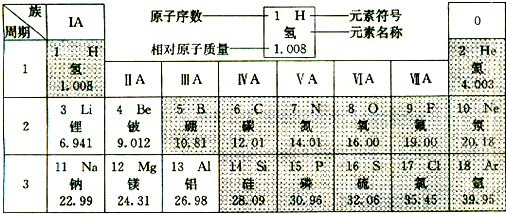
23、下图是元素周期表中的一部分.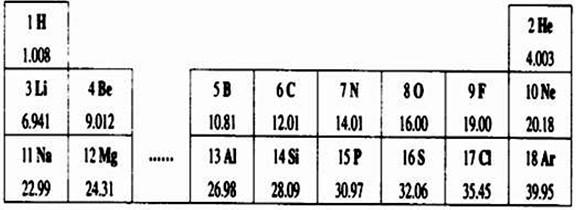
在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强.请回答:
(1)硅的相对原子质量为
(2)原子半径:钠
(3)与钠元素化学性质相似的元素为
(4)分析上表可发现:每一横行元素从左向右排列所遵循的一条规律是

在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强.请回答:
(1)硅的相对原子质量为
28.09
;原子序数为8的元素位于元素周期表的第
2
周期,元素符号为
O
,它属于
非金属
(填“金属”或“非金属”)元素.(2)原子半径:钠
>
镁(填“>”或“═”或“<”,下同),原子得电子能力:硫
<
氯.(3)与钠元素化学性质相似的元素为
锂
.(4)分析上表可发现:每一横行元素从左向右排列所遵循的一条规律是
每一横行,质子数逐渐增大
.分析:根据在元素周期表中,随原子序数的递增,原子结构中电子层数、最外层电子数发生规律性的变化,元素的种类(金属、非金属、稀有气体)和元素性质,也发生规律性的变化,解答本题.
解答:解:(1)在元素周期表中可查得硅的相对原子质量为28.09,可查得原子序数为8的元素位于元素周期表的第 2周期,元素符号为 O,属于非金属,
故答案为:28.09;2;O;非金属;
(2)根据在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强,
故答案为:>;<;
(3)根据元素周期表的规律最外层电子数相同的元素化学性质相似,故答案为:锂;
(4)在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子序数与质子数相等,
故答案为:每一横行,质子数逐渐增大.
故答案为:28.09;2;O;非金属;
(2)根据在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强,
故答案为:>;<;
(3)根据元素周期表的规律最外层电子数相同的元素化学性质相似,故答案为:锂;
(4)在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子序数与质子数相等,
故答案为:每一横行,质子数逐渐增大.
点评:本题考查了学生根据元素周期表的规律和所给信息去解题能力.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
 12、元素周期表是学习化学的重要工具,下图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )
12、元素周期表是学习化学的重要工具,下图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )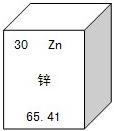 16、元素周期表是学习和研究化学的重要工具.请完成下列问题:
16、元素周期表是学习和研究化学的重要工具.请完成下列问题: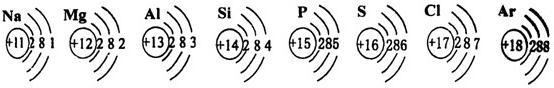
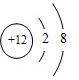

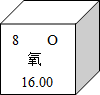 元素周期表是学习化学的重要工具.下图是元素周期表中的一格,从中获取的信息错误的是( )
元素周期表是学习化学的重要工具.下图是元素周期表中的一格,从中获取的信息错误的是( )