题目内容
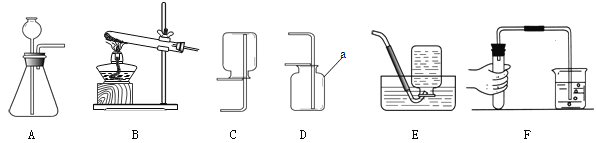
【题目】某兴趣小组用木炭还原氧化铜制取铜。该小组对生成的气体提出了质疑,根据碳与氧气反应后产物可能是CO2和CO,联想到碳与氧化铜反应是否有可能会产生CO。基于上述思考,为探究产物中气体的组成,设计如下实验:

Ⅰ.请写出A装置试管中的化学方程式: ⑽ 。
Ⅱ.装置B、D中盛放的足量的试剂名称及作用是 ⑾ 。
Ⅲ.若在 ⑿ 的现象,说明有一氧化碳气体生成。
Ⅳ.当装置B中的石灰水里不再冒气泡时,反应停止,待A装置中试管冷却后倒出残留的固体物,固体残留物中一定含有铜,可能还含有物质有 ⒀ 。(用化学式表示)
Ⅴ.兴趣小组对CO产生的原因进行了分析:
原因一:木炭和氧化铜在高温条件下直接发生反应生成CO和 Cu;
原因二:用化学方程式表示还可能产生CO的反应: ⒁ 。
【答案】Ⅰ⑽C +2CuO![]() 2Cu + CO2↑ 1
2Cu + CO2↑ 1
Ⅱ ⑾ 澄清石灰水,检验是否有二氧化碳生成,并除去二氧化碳
Ⅲ ⑿ C装置中黑色粉末变成亮红色,D装置中澄清石灰水变浑浊
Ⅳ ⒀ C或CuO
Ⅴ ⒁ C +CO2![]() 2CO
2CO
【解析】
试题分析:Ⅰ、碳还原氧化铜生成的是铜和二氧化碳:C +2CuO![]() 2Cu + CO2↑;
2Cu + CO2↑;
Ⅱ、该实验是要检验是否生成了一氧化碳,故要先将二氧化碳除去,再通过一氧化碳的还原性实验来验证一氧化碳的存在,故B装置中装的是澄清石灰水,目的检验是否有二氧化碳生成,并除去二氧化碳;
Ⅲ、若C装置中黑色粉末变成亮红色,D装置中澄清石灰水变浑浊,则证明生成了一氧化碳;
Ⅳ、碳还原氧化铜实验中碳粉或氧化铜可能是过量的,故剩余固体中可能含有碳或氧化铜;
Ⅴ、碳能与生成的二氧化碳固液生成一氧化碳:C +CO2![]() 2CO。
2CO。

练习册系列答案
相关题目