题目内容
【题目】按要求写出下列符号或符号表示的意义。
(1)3个二氧化碳分子_____________。
(2)7个钠离子_____________________。
(3)二氧化硫中硫元素显+4价_____________________。
(4)N表示①______________________,②______________________。
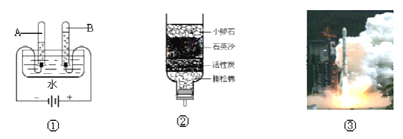
【答案】 3CO2 Na+ ![]() 氮元素 1个氮原子
氮元素 1个氮原子
【解析】(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则3个二氧化碳分子可表示为:3![]() ;(2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字。7个钠离子可表示为:7
;(2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字。7个钠离子可表示为:7![]() ;(3)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.二氧化硫中硫元素显+4价可表示为:
;(3)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.二氧化硫中硫元素显+4价可表示为: ![]() ;(4)根据元素符号的意义可知,N表示①氮元素;②表示一个氮原子。
;(4)根据元素符号的意义可知,N表示①氮元素;②表示一个氮原子。

【题目】某化学小组测定空气中氧气的体积分数。
(1)根据下图回答问题。
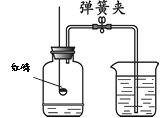
①红磷燃烧的文字表达式为_______________________。
②红磷燃烧时的现象是___________________________,冷却到室温打开止水夹后,观察到的现象是烧杯中的水_______________。
③冷却至室温后打开止水夹,发生上述现象的原因是_______________________________。
④实验结论:___________________________________________
(2)用四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数。
反应原理为:2Na2S4+O2+2H2O == 8S↓+4NaOH(氢氧化钠)。
小资料:四硫化钠(Na2S4)与氧气、水反应生成难溶于水的固体硫(S)和易溶于水的氢氧化钠。
【实验过程】
①取足量的四硫化钠固体加入试管中,再加入适量的水,迅速塞紧橡胶塞,充分振荡。测量液面至橡胶塞下沿的距离,记录数据h1(如图1所示)。
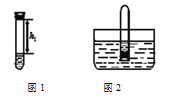
②将该试管插入水中(如图2所示),拔下橡胶塞,观察到_____________,塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2。理论上h2∶h1=______________。
③按照①和②再重复实验2次。3次实验数据如下表所示。
第1次 | 第2次 | 第3次 | |
h1/cm | 11.0 | 11.4 | 11.6 |
h2/cm | 8.7 | 9.1 | 9.2 |
根据第3次实验数据,计算空气中氧气的体积分数为________%(结果精确到 0.1%)。
【题目】下表是某科学研究小组探究影响反应速率部分因素的相关实验数据。
实验序号 | 过氧化氢溶液浓度 | 过氧化氢溶液体积/mL | 二氧化锰的用量/g | 收集氧气的体积/mL | 反应所需的时间/s |
① | 5% | 1 | 0.1 | 4 | 16.75 |
② | 15% | 1 | 0.1 | 4 | 6.04 |
③ | 30% | 5 | 0 | 2 | 49.21 |
④ | 30% | 5 | 0.1 | 2 | 10.76 |
(1)请写出过氧化氢分解的文字表达式____________________________________________________。
(2)通过实验________和实验________对比可知(填实验序号),化学反应速率与反应物的浓度有关;从实验③和④对比可知,化学反应速率与________________有关。
(3)为完成本实验,应选择下图所示气体发生装置和收集装置的组合是___________。(填序号)
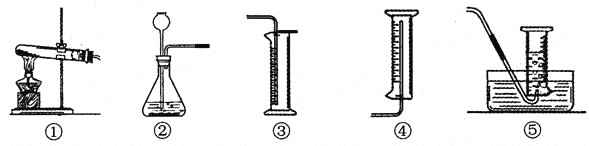
(4)【反思】过氧化氢在常温下分解缓慢,加入二氧化锰后反应明显加快。若要证明二氧化锰粉是否是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_____________和_____________是否改变。
过氧化氢生成氧气的快慢还与哪些因素有关?请你帮助他们继续探究。(只要求提出假设和实验方案)
【假设】_________________________________________。
【实验方案】_______________________________________________________________。