题目内容
反思、归纳与提升是化学学习的重要方法。对于复分解反应及其规律,通过反思与探索,同学们有了新的认识。请填写下文中横线上的空白。
【知识回顾】
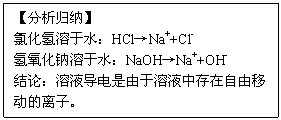
1.氯化氢气体、氢氧化钠固体不导电。
2.盐酸、氢氧化钠溶液能导电


【迁移运用】硫酸钠溶液能导电,原因是硫酸钠溶于水:Na2SO4→________。
【探索发现】
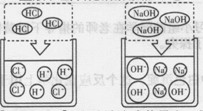
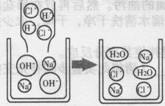
(1)氢氧化钠溶液与盐酸反应的微观示意图


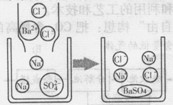
(2)硫酸钠溶液跟氯化钡溶液反应的微观示意图


(提示:生成硫酸钡白色沉淀)
(3)有气体生成的复分解反应,以Na2CO3+2HCl=2NaCl+H2O+CO2↑为例,反应实质:2H++CO32-→________________。
【总结规律】
上述复分解反应能发生的本质原因____________________________________。
【答案】【迁移运用】2Na++SO42-(1分,漏掉系数2不扣分)
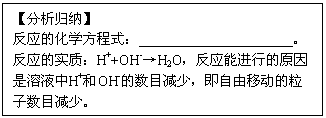
【探索发现】(1)NaOH+HCl=NaCl+H20(2分)
(2)BaCl2+Na2SO4=BaS04↓+2NaCl(2分),Ba2+和SO42- (1分,只写一种不得分)
(3)H20+CO2↑ (1分,只写一种不得分)
【总结规律】溶液中自由移动的离子的数目减少(1分,其它答案只要合理即得分)

练习册系列答案
相关题目








 有气体生成的复分解反应,以Na2CO3+2HCl=2NaCl+H2O+CO2↑为例,
有气体生成的复分解反应,以Na2CO3+2HCl=2NaCl+H2O+CO2↑为例,