题目内容
【题目】发酵粉是糕点的常见蓬松剂,成分一般是NH4HCO3、NaHCO3 . 某同学将发酵粉加入到一定量的氢氧化钙饱和溶液中,产生大量气泡和白色固体,溶液呈无色.
Ⅰ、为确定气体和固体及溶液的成分,该同学进行了如下的探究:
(1)将气体通入紫色石蕊试液中,石蕊试液变蓝色.则该气体为(写化学式),生成该气体的化学方程式是 .
(2)对白色固体做出如下猜测并进行实验:
【猜测】①白色固体是CaCO3;②;③白色固体是CaCO3和Ca (OH)2 .
【实验】取洗净后的白色固体,加入足量的水,滴入酚酞,无明显变化,则白色固体一定是 .
(3)将所得溶液分为两份:
①一份中加足量的稀盐酸,无气体;
②在另一份中通入足量的CO2后,滴入酚酞.生成白色沉淀且溶液呈红色.则原溶液中有溶质、(写化学式).
(4)Ⅱ、为确定发酵粉成分含量,该同学进行了定量实验:
称取干燥的白色固体10 g,充分加热至质量不再改变为止,称得残留固体质量为 5.3g.则发酵粉中NH4HCO3与NaHCO3的质量比为 .
【答案】
(1)氨气,2NH4HCO3+Ca(OH)2=2NH3↑+CaCO3↓+2H2O
(2)Ca(OH)2,CaCO3
(3)Ca(OH)2,NaOH
(4)4:21
【解析】解:将气体通入紫色石蕊试液中,石蕊试液变蓝色.则该气体为氨气,因为反应物中有NH4HCO3,生成该气体的化学方程式是2NH4HCO3+Ca(OH)2=2NH3↑+CaCO3↓+2H2O;
【猜测】①白色固体是CaCO3;②Ca(OH)2;③白色固体是CaCO3和Ca(OH)2.取洗净后的白色固体,加入足量的水,滴入酚酞,无明显变化,则白色固体一定是碳酸钙,因为酚酞没有变色,说明不含有氢氧化钙.将所得溶液分为两份:①一份中加足量的稀盐酸,无气体;说明不含有碳酸钙;②在另一份中通入足量的CO2后,滴入酚酞.生成白色沉淀且溶液呈红色.则原溶液中有溶质Ca(OH)2、NaOH,
设碳酸氢钠的质量为x.
2NaHCO3 | Na2CO3+CO2↑+H2O |
168 | 106 |
x | 5.3g |
列比例式得![]() =
=![]() ,x=8.4g;
,x=8.4g;
发酵粉中NH4HCO3与NaHCO3的质量比=(10g-8.4g):8.4g=4:21。
所以答案是:(1)NH3;2NH4HCO3+Ca(OH)2=2NH3↑+CaCO3↓+2H2O;(2)Ca(OH)2;CaCO3;(3)Ca(OH)2;NaOH;(4)4:21。
【考点精析】利用书写化学方程式、文字表达式、电离方程式和根据化学反应方程式的计算对题目进行判断即可得到答案,需要熟知注意:a、配平 b、条件 c、箭号;各物质间质量比=系数×相对分子质量之比.

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案【题目】下表中,有关量的变化图象与其对应叙述相符的是( )
A | B | C | D |
|
|
|
|
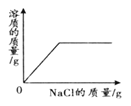
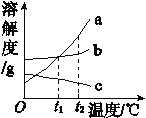
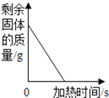
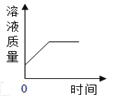
向接近饱和的NaCl溶液中加入固体NaCl | 将a、b、c三种物质的饱和溶液分别由t1 ℃升温至t2 ℃时,所得溶液中溶质质量分数的顺序a=b>c | 高温煅烧一定质量的石灰石 | 向足量的CuCl2中加入少量Fe |
A. A B. B C. C D. D