题目内容
【题目】在学习碳酸钠的性质的课堂上,老师在碳酸钠溶液中加入一定量的澄清石灰水产生白色沉淀,再滤出沉淀,引导同学们对滤液中溶质的成分进行探究。
同学们通过讨论认为溶质是NaOH、Na2CO3、Ca(OH)2中的一种或两种,其可能情况有三种:①NaOH;②NaOH和Na2CO3;③。
小伟同学设计了下列实验方案,请你帮助完成。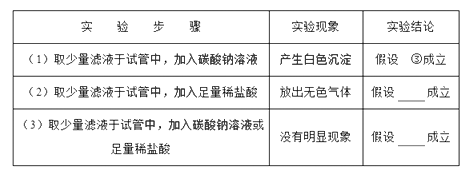
小强根据小伟设计的实验方案,在滤液中加入足量稀盐酸,观察到有大量气泡产生,产生该现象的化学方程式为。因此他得出的结论是只有假设成立,该假设成立说明老师做的实验是【选填“恰好完全反应”“Ca(OH)2过量”或“Na2CO3过量”】。
【答案】NaOH和 Ca(OH)2;②;①;Na2CO3+2HCl=2NaCl+CO2↑+H2O;②;Na2CO3过量
【解析】碳酸钠溶液与澄清石灰水反应会出现三种情况:其一,两溶液恰好完全反应,反应后的溶液中只含有氢氧化钠;其二,碳酸钠溶液过量,反应后的溶液中除生成的氢氧化钠外还含有未反应的碳酸钠;其三,澄清石灰水过量,反应后的溶液中除生成的氢氧化钠外还含有未反应的氢氧化钙;可采取向滤液样品中滴加碳酸钠溶液或澄清石灰水的方法,检验反应后溶液中是否含有澄清石灰水或碳酸钠;或根据碳酸钠、氢氧化钙的性质,选取稀盐酸利用碳酸钠能与稀盐酸反应放出二氧化碳进行检验。碳酸钠溶液与澄清石灰水可能恰好完全反应,形成氢氧化钠溶液;或者碳酸钠溶液过量,形成氢氧化钠与碳酸钠的混合溶液;或者澄清石灰水过量,形成氢氧化钠与氢氧化钙的混合溶液;故第③种猜想为:NaOH和Ca(OH)2;
取过滤后的滤液,分别继续滴加碳酸钠溶液或澄清石灰水,如果除氢氧化钠外还含有氢氧化钙或碳酸钠,则会有白色沉淀出现;采取在滤液中加入盐酸,有气泡产生,说明滤液中含有碳酸钠,则猜想②成立;取过滤后的滤液,分别继续滴加碳酸钠溶液或澄清石灰水,如果没有出现白色沉淀,说明恰好完全反应,则猜想①成立;在滤液中加入足量稀盐酸,观察到有大量气泡产生,说明滤液中含有碳酸钠,碳酸与盐酸反应放出二氧化碳,化学方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O;因此反应后的溶液为NaOH和Na2CO3的混合溶液,猜想②正确;说明所加入澄清石灰水量不足,碳酸钠过量。
故答案为:NaOH和 Ca(OH)2;②;①;Na2CO3+2HCl=2NaCl+CO2↑+H2O;②;Na2CO3过量
碳酸钠与氢氧化钙的反应有三种情况:恰好完全反应是生成碳酸钙和氢氧化钠,当碳酸钠过量时,溶质除了氢氧化钠还有未反应的碳酸钠,当氢氧化钙过量时,溶质为氢氧化钠和氢氧化钙,因此可采用向溶液中加碳酸钠或氢氧化钙的方法检测是否含有氢氧化钙或碳酸钠,根据碳酸钠和氢氧化钙的性质,利用稀盐酸进行检验

【题目】物质的性质决定用途.下列是物质的一些性质:①密度小,很稳定、②有吸附性、③有导电性、④易升华、⑤能与酸反应.请选择恰当的数字序号填空.
用途 |
|
|
|
|
|
性质 | (1)石墨 | (2)活性炭 | (3)氦气 | (4)碳酸氢钠 | (5)干冰 |

