题目内容
(2013?眉山)根据下列要求填空:
(1)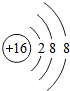 表示的是
表示的是
(2)质量分数大于1%的盐酸溶液常温下pH
(3)金属钛又称为21世纪金属,在各个领域都有重要用途.人造卫星和宇宙飞船上的天线是由钛镍形状记忆合金制造的.工业上生产钛是在高温下用熔融TiCl4与钠反应制得.请写出该反应的化学方程式
(1)
 表示的是
表示的是S2-
S2-
(填离子符号),其核电荷数为16
16
;(2)质量分数大于1%的盐酸溶液常温下pH
<
<
7(填“>”、“<”、“=”),向盛有盐酸的试管中滴入紫色石蕊试液,溶液变为红
红
色;(3)金属钛又称为21世纪金属,在各个领域都有重要用途.人造卫星和宇宙飞船上的天线是由钛镍形状记忆合金制造的.工业上生产钛是在高温下用熔融TiCl4与钠反应制得.请写出该反应的化学方程式
TiCl4+4Na
Ti+4NaCl
| ||
TiCl4+4Na
Ti+4NaCl
.
| ||
分析:(1)根据粒子的结构示意图分析;
(2)根据溶液的酸碱性与酸碱度的关系以及指示剂的变色情况分析;
(3)根据工业上制取钛的反应,写出反应的方程式.
(2)根据溶液的酸碱性与酸碱度的关系以及指示剂的变色情况分析;
(3)根据工业上制取钛的反应,写出反应的方程式.
解答:解:(1)由粒子的结构示意图可知,该微粒的质子数是16,核外电子数是18,离子的符号是S2-,核电荷数是16;
(2)盐酸的溶液显酸性,pH<7,能使紫色石蕊试液变为红色;
(3)工业上生产钛是在高温下用熔融TiCl4与钠反应制得,该反应的化学方程式是:TiCl4+4Na
Ti+4NaCl.
故答为:(1)S2-,16;(2)<,红; (3)TiCl4+4Na
Ti+4NaCl.
(2)盐酸的溶液显酸性,pH<7,能使紫色石蕊试液变为红色;
(3)工业上生产钛是在高温下用熔融TiCl4与钠反应制得,该反应的化学方程式是:TiCl4+4Na
| ||
故答为:(1)S2-,16;(2)<,红; (3)TiCl4+4Na
| ||
点评:本题涉及的知识点较多,但难度不大,属于基础的知识,应加强基础知识的学习.

练习册系列答案
相关题目