题目内容
废铜屑制硫酸铜,小花同学方案为铜与浓硫酸反应,其反应原理是:Cu+2H2SO4(浓)
CuSO4+X↑+2H2O.小朵同学方案为:2Cu+O2
2CuO,CuO+H2SO4=CuSO4+H2O.
则X是______(写化学式),较好的方案是______,其优点有(1)______,(2)______.
| ||
| ||
则X是______(写化学式),较好的方案是______,其优点有(1)______,(2)______.
根据反应前后元素的种类和数目不变,X的化学式为SO2
由反应可知:甲方案:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,
乙方案:2Cu+O2
2CuO;CuO+H2SO4(稀)═CuSO4+H2O,
制取相同量的硫酸铜时,方案甲消耗的硫酸比乙的多,并且制取过程中产生了污染大气的有毒气体SO2.
故答为:SO2,小朵;(1)不产生污染性气体,(2)硫酸利用率高;
由反应可知:甲方案:Cu+2H2SO4(浓)
| ||
乙方案:2Cu+O2
| ||
制取相同量的硫酸铜时,方案甲消耗的硫酸比乙的多,并且制取过程中产生了污染大气的有毒气体SO2.
故答为:SO2,小朵;(1)不产生污染性气体,(2)硫酸利用率高;

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
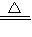 CuSO4+X↑+2H2O.小朵同学方案为:2Cu+O2
CuSO4+X↑+2H2O.小朵同学方案为:2Cu+O2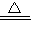 2CuO,CuO+H2SO4=CuSO4+H2O.
2CuO,CuO+H2SO4=CuSO4+H2O. CuSO4+X↑+2H2O.小朵同学方案为:2Cu+O2
CuSO4+X↑+2H2O.小朵同学方案为:2Cu+O2 2CuO,CuO+H2SO4=CuSO4+H2O.
2CuO,CuO+H2SO4=CuSO4+H2O.