题目内容
右图是某硫酸试剂瓶标签上的部分文字说明。
(1)取10 mL该硫酸可配制成9.8%的硫酸___________g。
(2)取适量该硫酸与锌反应可生成S02气体:Zn+2H2SO4(浓) ===ZnSO4+SO2↑+2H2O。反应一段时间后,还可能生成另一种气体,请解释其原因。

(1)184 (2)随着硫酸的消耗和水的生成,硫酸变稀,锌与稀硫酸反应能生成氢气。
解析:(1)10 mL 该硫酸含有硫酸的质量为: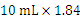 g/cm3×98%=18 .032 g。设配制含硫酸18.032 g的质量分数为9.8%的硫酸溶液的质量为x,则x×9.8%=18.032 g,解得x=184 g。
g/cm3×98%=18 .032 g。设配制含硫酸18.032 g的质量分数为9.8%的硫酸溶液的质量为x,则x×9.8%=18.032 g,解得x=184 g。

练习册系列答案
相关题目
右图是某硫酸试剂瓶标签上的部分文字说明。
 |
(1)取10mL该硫酸可配制成9.8%的硫酸 g。
(2)取适量该硫酸与锌反应可生成S02气体:Zn+2H22O4 (浓)=ZnSO4+SO2↑+2H2O。反应一段时间后,还可能生成另一种气体,请解释其原因。
 17、右图是某硫酸试剂瓶标签上的部分文字说明.
17、右图是某硫酸试剂瓶标签上的部分文字说明. 
