题目内容
化学课上,老师做了一个小实验:取一个烧杯,杯底放一支短蜡烛,并放入一些碳酸钙粉末.把蜡烛点燃,沿烧杯壁倒入一些盐酸,观察到碳酸钙 ,同时有 产生,然后蜡烛熄灭,蜡烛熄灭的原因是 .
【答案】分析:本题考查酸与碳酸盐反应实验现象的观察和二氧化碳的相关性质.
解答:解:因为盐酸和碳酸钙可以反应生成二氧化碳气体,所以看到碳酸钙粉末逐渐减少,且有大量气泡产生;因为二氧化碳密度比空气大,所以生成的二氧化碳会慢慢充满烧杯,二氧化碳气体不支持燃烧,所以蜡烛熄灭.
故答案为:减少;气泡;碳酸钙与盐酸反应生成CO2气体,充满烧杯,CO2气体不支持燃烧,所以蜡烛熄灭.
点评:实验的现象主要是利用看听闻尝摸,本题出现的现象都是看到的,同时要注意与反应原理相结合.
解答:解:因为盐酸和碳酸钙可以反应生成二氧化碳气体,所以看到碳酸钙粉末逐渐减少,且有大量气泡产生;因为二氧化碳密度比空气大,所以生成的二氧化碳会慢慢充满烧杯,二氧化碳气体不支持燃烧,所以蜡烛熄灭.
故答案为:减少;气泡;碳酸钙与盐酸反应生成CO2气体,充满烧杯,CO2气体不支持燃烧,所以蜡烛熄灭.
点评:实验的现象主要是利用看听闻尝摸,本题出现的现象都是看到的,同时要注意与反应原理相结合.

练习册系列答案
相关题目
化学课上,老师做了有趣的实验:向盛有蓝色硫酸铜溶液的试管中,滴加氢氧化钠溶液,产生蓝色沉淀,同时溶液由 蓝色变为无色.化学兴趣小组的同学就此展开了探究.
[提出问题1]硫酸铜溶液与氢氧化钠溶液反应生成什么物质?
[查阅资料]①下表是部分碱、盐在室温时溶解性表
| 离子 | OH- | SO | NO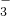 | Cl- |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Cu2+ | 不溶 | 溶 | 溶 | 溶 |
②硫酸钠溶液呈酸性
①根据资料和复分解反应发生的条件写出该反应的化学方程式________
②将上述溶液与沉淀分离采用的方法是________该操作中玻璃棒的作用是:________
[提出问题2]无色溶液中溶质的成分是什么?
[猜想假设]
猜想一:硫酸钠
猜想二:硫酸钠与硫酸铜
猜想三:硫酸钠与氢氧化钠
同学们经过讨论认为猜想________不成立,理由是:________
[实验探究]化学兴趣小组的同学通过以下实验验证了猜想三成立,请 你完成实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| 猜想三成立 |
 和水⑤硝酸铵和水
和水⑤硝酸铵和水