题目内容
【题目】如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论不正确的是
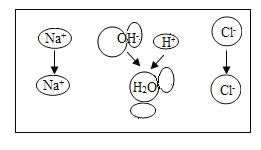
A.反应后溶液能使无色酚酞变红
B.反应前后溶液中Na+和C1-的个数不变
C.该反应的实质是H+和OH-结合生成水分子
D.反应前后的溶液均能导电
【答案】A
【解析】
A、氢氧化钠溶液与稀盐酸恰好完全反应生成氯化钠和水,氯化钠溶液显中性,不能使无色酚酞变红,故错误;
B、由反应的微观示意图可知,氢氧化钠和盐酸的反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成了水分子,反应前后溶液中Na+和C1-的个数不变,故正确;
C、氢氧化钠和盐酸的反应为中和反应,反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成了水分子,故正确;
D、反应前氢氧化钠溶液中含有钠离子、氢氧根离子,盐酸中含有氢离子、氯离子,反应后溶液中存在钠离子和氯离子,所以反应前后的溶液均能导电,故正确。
故选:A。

 名校练考卷期末冲刺卷系列答案
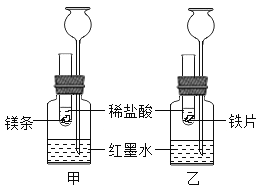
名校练考卷期末冲刺卷系列答案【题目】为探究酸、碱、盐的化学性质,某兴趣小组做了如下实验。试回答下列问题:
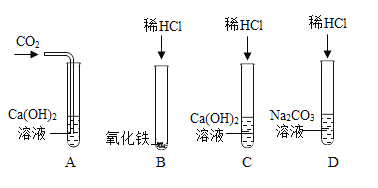
(1)试管A中的现象是__________;
(2)试管B中反应的化学方程式为__________________;
(3)甲同学把反应后C、D试管中的废液倒入一只烧杯中,观察到先有气泡产生,后有白色沉淀生成;过滤后得到白色沉淀和无色滤液。甲同学欲探究无色滤液中溶质的成分。
(提出问题)无色滤液中的溶质是什么?
(作出猜想)猜想Ⅰ:NaCl;
猜想Ⅱ:NaCl和CaCl2;
猜想Ⅲ:NaCl 和Na2CO3;
猜想Ⅳ:NaCl、CaCl2 和Na2CO3。
小明认为猜想Ⅳ一定不成立,原因是________________。
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
(1)取少量滤液于试管中,滴加少量Na2CO3溶液 | 无明显现象 | 猜想___成立 |
(2)取少量滤液于试管中,滴加少量_____ | 有气泡产生 |