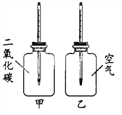
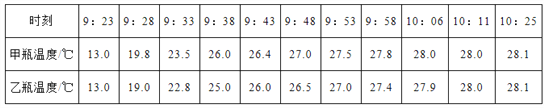
题目内容
【题目】现将10.6g某固体混合物样品与足量盐酸起反应,收集到4.4gCO2。若此混合物是由MgCO3、Na2CO3、CaCO3和K2CO3中的3种物质所组成,则该混合物组成不可能是( )
A. Na2CO3、CaCO3和K2CO3 B. Na2CO3、CaCO3和MgCO3
C. Na2CO3、MgCO3和K2CO3 D. CaCO3、K2CO3 和MgCO3
【答案】A
【解析】假设该混合物样品全是Na2CO3;设它反应生成的二氧化碳的质量为x,
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
10.6g x
![]()
x=4.4g
同理可得,同样质量(即10.6g)的MgCO3、CaCO3和K2CO3与足量盐酸完全反应后,生成的二氧化碳的质量分别为:5.6g、4.7g和3.4g;
A、由于Na2CO3、CaCO3和K2CO3与足量盐酸完全反应后,生成的二氧化碳的质量分别为:4.4g、4.7g和3.4g,是有可能平均到4.4g的;所以,该混合物组成是有可能的,但不符合题意,错误;
B、由于Na2CO3、CaCO3和MgCO3与足量盐酸完全反应后,生成的二氧化碳的质量分别为:4.4g、4.7g和5.6g,是不可能平均到4.4g的,并且肯定要大于4.4g,但小于5.6g;所以,该混合物组成是不可能的;正好符合题意,正确;
C、由于Na2CO3、K2CO3和MgCO3与足量盐酸完全反应后,生成的二氧化碳的质量分别为:4.4g、3.4g和5.6g,是有可能平均到4.4g的;所以,该混合物组成是有可能的;但不符合题意,错误;
D、由于CaCO3、K2CO3和MgCO3与足量盐酸完全反应后,生成的二氧化碳的质量分别为:4.7g、3.4g和5.6g,是有可能平均到4.4g的;所以,该混合物组成是有可能的;但不符合题意,错误。故选B。

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案【题目】为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质。其原理是把蛋白质中的氮元素完全转化成氨气(化学式为NH3),再用稀硫酸吸收氨气,反应的化学方程式:2NH3+H2SO4=(NH4)2SO4
现取该牛奶样品30 mL,用“盖尔达法”分解其中的蛋白质,产生的氨气用9.5 g溶质质量分数为4.9%的稀硫酸恰好完全吸收。计算并回答下列问题:
(1)产生氨气的质量是多少克?(计算结果精确到0.01 g,下同)
(2)30 mL牛奶中含氮元素的质量是多少克?
(3)下图是该牛奶包装标签的部分内容。已知牛奶中的蛋白质含氮元素的质量分数为16%,请你通过计算确定,该牛奶样品中蛋白质的含量是否达到了包装标签所标示的蛋白质的质量标准。
配料:鲜牛奶 保质期:8个月 净含量:250 mL/盒 营养成分:(每100 mL) 钙≥0.11 g 脂肪≥3.30 g 蛋白质≥2.90 g |