题目内容
【题目】下图为KNO3和某物质M在不同温度下配成饱和溶液时,所需溶质和溶剂的质量关系。
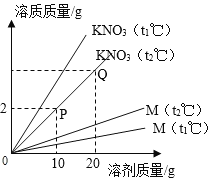
(1) t2℃时,KNO3的溶解度为____________________。
(2) P点处KNO3溶液的溶质质量分数为________________。 (精确到0.1%)
(3) Q点的纵坐标为________________。
(4)下列描述错误的是________________(填序号) 。
A 物质M的溶解度随温度的升高而减小
B 向10g水中加入2g KNO3,溶液质量一定为12g
C t2℃时,KNO3溶液的溶质质量分数一定大于M溶液的溶质质量分数
D t2℃时,将KNO3溶液恒温蒸发100g水,有晶体析出,则析出晶体的质量小于或等于20g
【答案】20g 16.7% 4 BC
【解析】
(1) 根据图示,t2℃时10g水中加入2g KNO3恰好配成饱和溶液,则100g水中加入20g KNO3也能配成饱和溶液。根据固体溶解度的含义可得,t2℃时KNO3的溶解度为20g。
(2)根据图示,P点处KNO3溶液的溶质质量分数为:![]() 。
。
(3) 因为P、Q两点的温度相同,P点10g溶剂中加入2g KNO3恰好配成饱和溶液,Q点溶剂质量是20g,则需加入4g KNO3才能配成饱和溶液,因此Q点的纵坐标为:4。
(4) A、根据图示信息,物质M的溶解度随温度变化的趋势与硝酸钾的溶解度随温度变化的趋势相反。图中显示同样多的溶剂中,硝酸钾在t1℃时溶解的质量大于t2℃,根据硝酸钾的溶解度随温度升高而增大的规律,可见t1℃高于t2℃。图中显示,物质M在同样多的溶剂中,t1℃时溶解的质量少于t2℃,说明物质M的溶解度随温度的升高而减小,描述正确;
B、由于温度不确定,硝酸钾的溶解度也不确定,因此向10g水中加入2g KNO3,如果全部溶解,溶液质量为12g,如果不能全部溶解,所得溶液质量小于12g,描述错误;
C、因为没有指明溶液是否饱和,t2℃时KNO3溶液的溶质质量分数不一定大于M溶液的溶质质量分数,描述错误;
D、t2℃时,如果是硝酸钾的饱和溶液,将溶液恒温蒸发100g水,析出晶体质量为20g,如果是硝酸钾的不饱和溶液,将溶液恒温蒸发100g水,如果有晶体析出,析出晶体的质量小于20g,描述正确。故四种说法中描述错误的是BC。

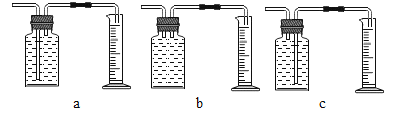
【题目】某校实验室有一瓶久置的铁屑,其成分是铁、氧化铁和水。为测定其中各成分的质量分数,某兴趣小组按下图所示装置进行实验(装置气密性良好;固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
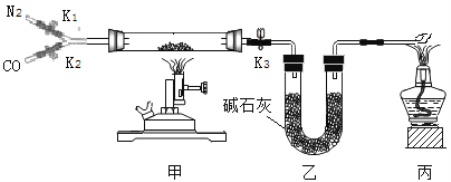
部分实验步骤如下:
Ⅰ.称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
II.连接好装置。缓缓通入N2,点燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ.再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
实验数据记录如下表:
硬质玻璃管 | 硬质玻璃管和样品 | 步骤II硬质玻璃 管和剩余固体 | 步骤步骤Ⅲ硬质玻璃 管和剩余固体 | |
质量 | m1 | m2 | m3 | m4 |
请回答下列问题:
(1)步骤Ⅲ丙处酒精灯的作用是____________。
(2)步骤Ⅲ硬质玻璃管中反应的化学方程式为________。
(3)样品中氧化铁的质量分数为_____(用m1、m2、m3、m4的代数式表示)。若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将______(填“偏大”“偏小”或“不变”)。
(4)有关样品,下列说法正确的是_____(填字母标号)。
A样品中氢元素的质量为1/9(m2-m3) B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1 D样品中氧元素的质量为m3-m4