题目内容
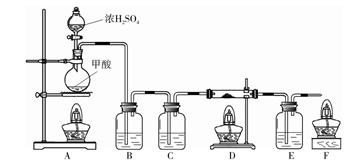
某同学用下图所示装置制取纯净、干燥的CO,并测定某氧化铜和铜的混合物中铜单质的含量。
资料
①常温下,甲酸(HCOOH)是无色易挥发的液体,在浓硫酸作用下易分解。
甲酸分解的化学方程式为:HCOOH 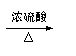 CO↑+ H2O。
CO↑+ H2O。
②浓硫酸具有吸水性,难挥发,常用作干燥剂。

(1)E中澄清石灰水变浑浊,反应的化学方程式是 。
(2)装置B的作用是 ,装置C中的试剂是 。点燃装置F中酒精灯的目的是
。
(3)实验结束时,熄灭酒精灯的顺序是 (填对应装置序号)。
(4)若称取该混合物5.0 g,充分反应后,玻璃管中剩余固体的质量为4.8 g。原混合物中铜单质的质量分数为 。
(1)CO2 + Ca(OH) 2 = CaCO3↓+ H2O
(2)除去挥发出来的甲酸 浓硫酸 处理尾气,防止空气污染
(3)DAF (4)80%

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目

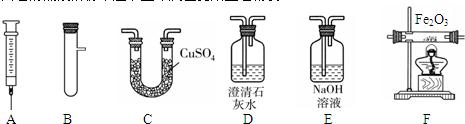

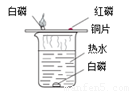
 CO↑+ H2O。
CO↑+ H2O。