题目内容
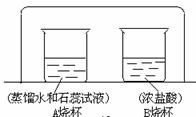
如下图所示,老师在课堂上演示了一个有趣的实验:在一只洁净的小烧杯A中装入30 mL蒸馏水,再滴入2~3滴石蕊试液;在小烧杯B中装入30 mL浓盐酸;用一个玻璃水槽把A、B两个烧杯罩在一起,一会儿就看到A烧杯中的溶液变成了红色.
同学们对上述现象看法不一,有以下两种猜测:
第一种:A烧杯中的蒸馏水使石蕊试液变红
第二种:B烧杯中的浓盐酸挥发出一种气体,溶解到A烧杯的溶液中,使溶液变成红色
(1)你认为哪种猜测是正确的?如果你不同意以上两种猜测,请给出你的猜测.
________________________________________________________________________
(2)请你设计实验方案,说明(1)中你的猜测.提供的实验用品:烧杯、试管、胶头滴管、滤纸;蒸馏水、石蕊试液、浓盐酸、氯化氢气体等.
实验(简述实验内容和方法) | 观察到的实验现象 |
(3)通过实验探索,对这个趣味实验,你得出的结论是___________________________.
(1)第二种
(2)
| 实验内容、方法 | 观察到的实验现象 | |
| 实验1 | 用洁净的烧杯取20 mL蒸馏水,滴入2~3滴石蕊试液,观察现象.(或将该烧杯单独罩在玻璃水槽里放置一段时间) | 蒸馏水不变色 |
| 实验2 | ①向滤纸上滴加石蕊然后放在盛浓盐酸烧杯上方 ②或打开盛装浓盐酸的试剂瓶,观察 ③或闻B烧杯浓盐酸的气味 | 滤纸变红出现白雾能闻到刺激性气味 |
| 实验3 | 将氯化氢气体通入含有石蕊试液的蒸馏水中,观察 | 溶液变红 |
| 实验4 | 向盐酸中滴入紫色石蕊试液,观察 | 溶液变红 |
(3)结论1:盐酸能使石蕊试液变红;结论2:蒸馏水不能使石蕊试液变红;结论3:浓盐酸具有挥发性.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
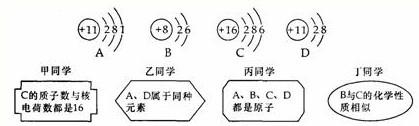

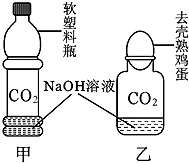 (2008?怀柔区一模)化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,观察到前者变浑浊,后者无明显现象,同学们展开了探究.
(2008?怀柔区一模)化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,观察到前者变浑浊,后者无明显现象,同学们展开了探究.