题目内容
在托盘天平的两边各放一只盛有足量相同质量、相同质量分数稀盐酸的烧杯,调至平衡,然后向左边烧杯中加⒌6g铁,欲使天平再次保持平衡,应向右边烧杯中加入( )
| A、6g镁 | B、⒌6g铜 |
| C、⒌4g氧化钙 | D、10g碳酸钙 |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:首先应分清楚相关的化学变化,再利用要使天平再次平衡需保证两边质量增加的量要相等,利用此知识可解决相关的问题.
解答:解:设5.6g铁与足量盐酸反应生成氢气的质量为x
Fe+2HCl=H2↑+FeCl2
56 2
5.6g x
=
x=0.2g
因此,天平左盘增加的质量为:5.6g-0.2g=5.4g,要使天平平衡,右盘增加的质量也应为5.4g.
A、设6g镁与足量盐酸反应生成氢气的质量为m,
Mg+2HCl=H2↑+MgCl2
24 2
6g m
=
m=0.5g
则增加的质量为:6g-0.5g=5.5g,不符合;
B、铜不与盐酸反应,因此,右盘增加的质量为5.6g,不符合;
C、氧化钙会与盐酸反应,但无气体跑出,因此右边烧杯加入5.4g氧化钙,就增加5.4g,符合题意;
D、设10g碳酸钙与足量盐酸反应生成二氧化碳的质量为n,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
10g n
=
n=4.4g
则增加的质量为:10g-4.4g=5.6g,不符合.
故选C.
Fe+2HCl=H2↑+FeCl2
56 2
5.6g x
| 56 |
| 2 |
| 5.6g |
| x |
x=0.2g
因此,天平左盘增加的质量为:5.6g-0.2g=5.4g,要使天平平衡,右盘增加的质量也应为5.4g.
A、设6g镁与足量盐酸反应生成氢气的质量为m,
Mg+2HCl=H2↑+MgCl2
24 2
6g m
| 24 |
| 2 |
| 6g |
| m |
m=0.5g
则增加的质量为:6g-0.5g=5.5g,不符合;
B、铜不与盐酸反应,因此,右盘增加的质量为5.6g,不符合;
C、氧化钙会与盐酸反应,但无气体跑出,因此右边烧杯加入5.4g氧化钙,就增加5.4g,符合题意;
D、设10g碳酸钙与足量盐酸反应生成二氧化碳的质量为n,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
10g n
| 100 |
| 44 |
| 10g |
| n |
n=4.4g
则增加的质量为:10g-4.4g=5.6g,不符合.
故选C.
点评:此题是一道天平知识考查题,解决的关键是分清两边的反应,利用天平平衡的原理进行解题.

练习册系列答案
相关题目
欲中和氯化钙溶液中少量的盐酸,在没有指示剂的条件下应选用的试剂是( )
| A、石灰石粉末 |
| B、生石灰粉末 |
| C、熟石灰粉末 |
| D、硝酸银溶液 |
化合物XY和ZY2中Y的质量分数分别为40%与50%,则化合物XZY4中X的质量分数为( )
| A、20% | B、30% |
| C、40% | D、50% |
我市在市郊建立了首个垃圾处理厂,实现了生活垃圾的无害化和资源化处理.2008年4月11日从各乡镇运来了第一批垃圾,在这批垃圾中,含废铝线、一次性塑料餐具、果皮、碎玻璃等.其中属于合成材料的是( )
| A、废铝线 | B、一次性塑料餐具 |
| C、果皮 | D、碎玻璃 |
下列化学实验操作正确的是( )
A、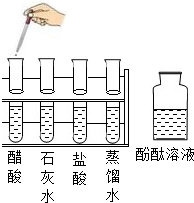 |
B、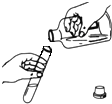 |
C、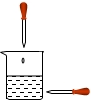 |
D、 |
下列实验基本操作正确的是( )
A、给试管里的液体加热时,液体应超过容积的
| ||
| B、稀释浓硫酸时,应将水慢慢注入浓硫酸里 | ||
| C、给试管加热时,应用手拿住试管夹的短柄 | ||
| D、将玻璃导管插入单孔橡皮塞时,应先用水润湿导管口 |
下列说法正确的是( )
| A、NaOH和MgO的混合物中氧的质量分数为40%,NaOH和MgO的质量比为任意值 |
| B、一定量的氯化钠溶液恒温蒸发5克水,析出a克晶体;再蒸发5克水,又析出b克晶体,a与b一定相等 |
| C、用H2完全还原一定质量的CuO,参加反应的H2与通入的H2质量一定相等 |
| D、将98%的浓H2SO4稀释成49%的稀H2SO4,加入水的质量与浓硫酸质量一定相等 |