题目内容
【题目】用化学方程式解释下列反应原理。
(1)正常雨水的pH≈5.6的原因_____。
(2)用石灰乳刷墙,墙壁会“出汗”_____。
【答案】CO2+H2O=H2CO3 CO2+Ca(OH)2═CaCO3↓+H2O
【解析】
(1)空气中的二氧化碳能与雨水反应生成碳酸,所以正常的雨水中含有碳酸,其pH≈5.6;故填:CO2+H2O=H2CO3;
(2)石灰乳中的氢氧化钙与空气中的二氧化碳反应生成碳酸钙沉淀和水,所以墙壁会“出汗”,故填:CO2+Ca(OH)2═CaCO3↓+H2O。

练习册系列答案
相关题目
【题目】小明在室温20℃时探究硝酸钾溶于水的情况。已知硝酸钾在不同温度下的溶解度如表所示:
温度/℃ | 10 | 20 | 60 | 100 |
溶解度/g | 20.9 | 31.6 | 110 | 246 |
A烧杯盛有20mL水,他进行了如下实验: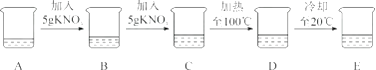
整个过程溶剂的量不变,根据有关资料回答问题:
(1)A→B、B→C操作中均需用到(填仪器名称);
(2)上述实验过程中属于饱和溶液的是(填字母,下同);
(3)在B,C,D,E中,溶液的溶质质量分数最小是;
(4)现在需要配制溶质质量分数为60%的硝酸钾饱和溶液,温度必须。