题目内容
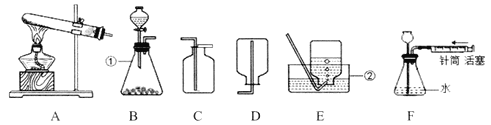
【题目】如图是实验室常用的实验仪器与装置,根据所学知识回答下列问题:
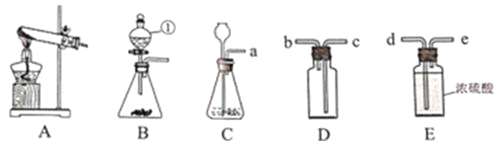
(1)写出图中编号仪器名称:①_____。
(2)用A装置制取氧气时,反应的化学方程式为_____。若用装置B制取氧气则反应的化学方程式为_____,装置B和装置C比较优点是_____。
(3)实验室制取二氧化碳的化学方程式为_____,若要收集一瓶干燥的二氧化碳气体,整套装置导管接口的正确连接顺序是a→_____(依次填导管接口,用a、b、c…表示)。
【答案】分液漏斗 2KMnO4![]() K2MnO4+MnO2+O2↑ 2H2O2
K2MnO4+MnO2+O2↑ 2H2O2![]() 2H2O+O2↑ 可以控制化学反应的速率 CaCO3+2HCl=CaCl2+H2O+CO2↑ d→e→c
2H2O+O2↑ 可以控制化学反应的速率 CaCO3+2HCl=CaCl2+H2O+CO2↑ d→e→c
【解析】
(1)仪器①是分液漏斗;故填:分液漏斗;
(2)装置A是固体加热型,且试管口处有一团棉花,所以是加热高锰酸钾制氧气,同时生成锰酸钾和二氧化锰;装置B适用于固液常温下制取气体,即过氧化氢在二氧化锰的催化作用下生成水和氧气;装置B和装置C比较优点是可以控制化学反应的速率;故填:2KMnO4![]() K2MnO4+MnO2+O2↑;2H2O2
K2MnO4+MnO2+O2↑;2H2O2![]() 2H2O+O2↑;可以控制化学反应的速率;
2H2O+O2↑;可以控制化学反应的速率;
(3)实验室制取二氧化碳可以用大理石或石灰石(主要成分是碳酸钙)和稀盐酸反应,生成氯化钙、水和二氧化碳,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;用浓硫酸干燥气体时,气体从长管进入,因为二氧化碳的密度比空气大,用装置D收集二氧化碳时,二氧化碳应从长管进入;故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;d→e→c。

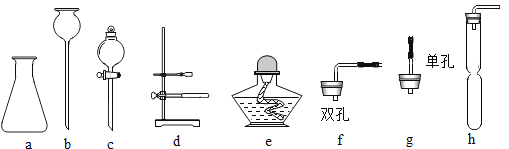
【题目】下列实验设计不能达到实验目的的是
选项 | A | B | C | D |
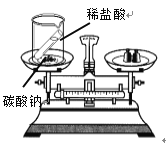
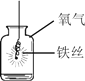
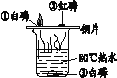
实验 目的 | 验证质量守恒定律 | 验证铁丝能在 氧气中燃烧 | 验证与氧气接触是燃烧的条件之一 | 鉴别NaCl、NaOH和 稀盐酸三种溶液 |
实验 方案 |
|
|
|
|
A. AB. BC. CD. D
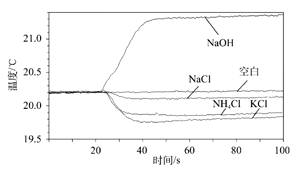
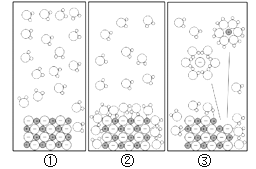
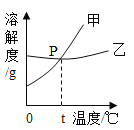
【题目】如表是NaCl和KNO3在不同温度时的溶解度,其变化趋势如图所示,下列推理合理的是( )
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
A. 100g水里最多能溶解KNO331.6g
B. 表示NaCl的溶解度曲线是甲
C. 温度t的范围可能在20℃﹣30℃之间
D. 不饱和溶液变为饱和溶液,溶质的质量分数增大