题目内容
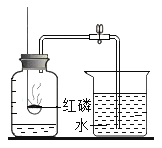
【题目】今年参加的化学实验考查的题目是“铵盐的检验”,试回答下列问题
(1)假设样品为氯化铵,试写出实验过程中发生反应的化学方程式_____.
(2)如图为紫薇同学检验铵根离子的操作图,请指出他被扣两分的原因

序号 | 扣分原因 |
1 | _____ |
2 | _____ |
(3)小康同学在实验前忘记把红色石蕊试纸用水润湿,但是当试管内的液体加热煮沸一会儿后,试纸也逐渐变成蓝色,你认为主要的原因是_____
(4)你认为假如实验室暂时没有找到红色石蕊试纸,可以临时代替物品有_____.
【答案】NH4Cl+NaOH![]() NaCl+H2O+NH3↑ 试管内液体太多 加热时大拇指按着试管夹的短柄 水蒸气逐渐把试纸湿润 pH 试纸
NaCl+H2O+NH3↑ 试管内液体太多 加热时大拇指按着试管夹的短柄 水蒸气逐渐把试纸湿润 pH 试纸
【解析】
(1)铵盐的检验:将样品放入试管加热,用湿润的红色石蕊试纸放在试管口,湿润红色石蕊试纸会变蓝色,证明产生的气体是氨气,证明该盐中含有铵根离子,有关反应的化学方程式是NH4Cl+NaOH![]() NaCl+H2O+NH3↑;
NaCl+H2O+NH3↑;
(2)图中错误有试管内液体太多,加热时大拇指按着试管夹的短柄;
(3)当试管内的液体加热煮沸一会儿后,水蒸气逐渐把试纸湿润,因此试纸也逐渐变成蓝色;
(4)可以用pH试纸替代红色石蕊试纸,检测物质的酸碱性;

 阅读快车系列答案
阅读快车系列答案【题目】长郡双语实验中学化学兴趣小组的同学将氢氧化钠溶液和稀硫酸混合,没有观察到明显的现象,他们对此提出了如下问题并进行了相应探究:
问题一:二者之间是否发生了反应?他们设计了如下方案证明二者之间确实发生了反应:
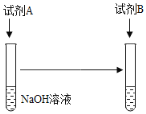
(1)可以选择的试剂组合有____________(填序号)。
①试剂A:足量稀硫酸,试剂B:MgCl2溶液
②试剂A:足量稀硫酸,试剂B:铁粉
③试剂A:少量稀硫酸,试剂B:MgCl2溶液
④试剂A:少量稀硫酸,试剂B:铁粉
(2)小玮认为:若选用_________溶液,不管加入顺序如何,只需控制加入稀硫酸的量也能证明二者发生了反应。
问题二:反应后溶液中溶质有哪些?
(猜想假设)猜想一:只有Na2SO4;猜想二:Na2SO4和NaOH;猜想三:Na2SO4和H2SO4。
(查阅资料)①Na2SO4溶液显中性,②Na2SO4+BaCl2=BaSO4↓+2NaCl。
(实验操作)分别取少量反应后的溶液于试管中,进行如下实验:
实验编号 | 实验过程 | 实验现象 |
① | 加入酚酞溶液 | 不变红 |
② | 加入少量BaCl2溶液 | 产生白色沉淀 |
③ | 加入少量(3)______溶液 | 没有气泡产生 |
(实验结论)猜想一成立。
(实验反思)小光认为,实验(4)________(填实验编号)可省略。小娟取少量反应后的溶液中于试管中,加入红色固体(5)___________(填化学式),观察到红色固体不溶解,也得出了相同结论。
【题目】将一定量的丙烷(C3H8)和氧气置于一个密闭的容器中引燃并充分反应,测得反应前后各物质的质量如表所示,下列判断不正确的是( )
物质 | C3H8 | O2 | H2O | CO2 | X |
反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
A.表中a的值一定是5.6
B.若8.8g丙烷完全反应,则生成14.4g水
C.生成物X中一定含有氢元素
D.若4.4g丙烷与16.0g氧气充分反应,则无X生成