题目内容
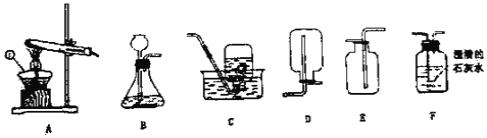
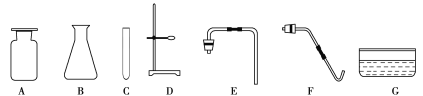
【题目】请结合下图回答问题:
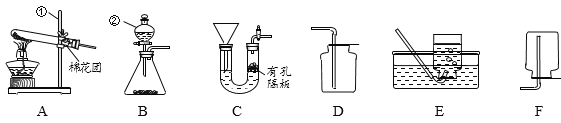
(1)仪器名称:②_____。
(2)若用A装置制备氧气,则反应的化学方程式为_____。若经检查该装置漏气,试简述检查漏气部位的方法:_____。
(3)实验室制取CO2,应选择的发生装置是或C(选填序号),C装置与该装置比较,优点是_____。该反应的化学方程式为_____。某小组用该装置制取CO2,经检查装置气密性良好,实验操作均正确,但实验中一直收集不到CO2,产生此现象的原因可能是_____。
(4)某化学兴趣小组欲探究金属的相关性质,请配合该组同学完成相关实验
①稀释浓硫酸:现有98%的浓硫酸,欲配制19.6%的稀硫酸10g,需水_____g,稀释的操作方法是_____。
②取两支试管,分别加入适量稀硫酸,将形状完全相同的铁片、铜片分别插入所配制的稀硫酸中,_____表面无明显现象,说明铁的活泼性比铜强;
③欲验证铁和铜的活泼性,还可选用的两种试剂是_____、_____。
【答案】分液漏斗 ![]() 导气管处连接注射器,并在可能漏气的部分涂上肥皂水,向试管内通入空气,产生肥皂泡部位漏气 能控制反应的进行与停止
导气管处连接注射器,并在可能漏气的部分涂上肥皂水,向试管内通入空气,产生肥皂泡部位漏气 能控制反应的进行与停止 ![]() 装置漏气 8g 将浓硫酸沿着烧杯壁缓缓倒入到水中,同时用玻璃棒不断搅拌 铜 铁片 硫酸铜溶液(合理即可)
装置漏气 8g 将浓硫酸沿着烧杯壁缓缓倒入到水中,同时用玻璃棒不断搅拌 铜 铁片 硫酸铜溶液(合理即可)
【解析】
(1)仪器②名称是分液漏斗;
(2)若用A装置制备氧气,反应的条件是加热,管口有一团可棉花,则制氧气的药品是高锰酸钾,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:![]() ;若经检查该装置漏气,检查漏气部位的方法在导气管处连接注射器,并在可能漏气的部分涂上肥皂水,向试管内通入空气,产生肥皂泡部位漏气;
;若经检查该装置漏气,检查漏气部位的方法在导气管处连接注射器,并在可能漏气的部分涂上肥皂水,向试管内通入空气,产生肥皂泡部位漏气;
(2)用C装置制二氧化碳时,将大理石或石灰石放在有孔隔板上,从漏斗处加入盐酸,盐酸与大理石或石灰石接触,产生二氧化碳,关闭活塞,气体不能导出,右管内的气压增大,导致右管中盐酸液面下降,固体与液体脱离接触,反应停止,打开活塞气体导出,右管内的气压下降,右管内的液面上升,固体与液体接触,反应进行。C装置与该装置比较,优点是能控制反应的进行与停止;实验室制取二氧化碳,是在常温下,用大理石或石灰石和稀盐酸制取的,大理石或石灰石的主要成分是碳酸钙,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学方程式为:![]() ;实验操作均正确,但实验中一直收集不到CO2,产生此现象的原因可能是装置漏气;
;实验操作均正确,但实验中一直收集不到CO2,产生此现象的原因可能是装置漏气;
(4)①设需要浓硫酸的质量为x,由于稀释过程中溶质的质量不变,则有:19.6%×10g=98%×x,x=2g,需要水的质量=10g-2g=8g;由于浓硫酸溶于水放出大量的热,且本身密度大于水,所以稀释浓硫酸的正确操作为将浓硫酸沿着烧杯壁缓缓倒入到水中,同时用玻璃棒不断搅拌;
②金属若能与硫酸反应产生氢气,则活动性大于氢,若不能反应则活动性小于氢。取两支试管,分别加入适量稀硫酸,将形状完全相同的铁片、铜片分别插入所配制的稀硫酸中,铜表面无明显现象,说明铁的活泼性比铜强;铁能与硫酸铜反应生成硫酸亚铁和铜。欲验证铁和铜的活泼性,还可选用的两种试剂是铁片和硫酸铜溶液(合理即可)。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案【题目】MgSO4和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是( )
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度 S/g | MgSO4 | 33.7 | 38.9 | 44.5 | 50.6 | 54.6 | 55.8 |
Na2SO4 | 19.5 | 40.8 | 48.8 | 47.5 | 45.3 | 44.8 | |

A. 甲为Na2SO4
B. t3℃应介于40℃~50℃之间
C. t4℃乙的饱和溶液,降温到t1℃的过程中,一直有晶体析出
D. b、c点乙的饱和溶液溶质质量分数相等,且大于a点甲的饱和溶液溶质质量分数