题目内容
【题目】合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步做出了巨大贡献。合成氨工艺的主要流程如下: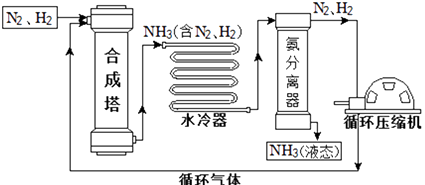
(1)合成塔中的反应必须在高温、高压、催化剂条件下进行,该反应的符号表达式是:。
(2)生产过程中可重复使用的物质是(填化学式)。
(3)根据表中的数据回答问题。
物质 | H2 | N2 | O2 | NH3 |
沸点/℃(1.01×105 Pa) | –252 | –195.8 | –183 | –33.35 |
在1.01×105 Pa时,要将产物NH3与N2、H2分离开来,最适宜的温度应该控制在℃。
(4)下图是合成塔中发生反应的微观粒子示意图: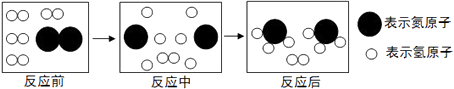
由图可知两种反应物N2与H2的分子个数比为;该反应中的最小粒子是(填写化学符号)。
【答案】
(1)N2+3H2 ![]() 2NH3
2NH3
(2)N2、H2
(3)–33.35
(4)1:3,N、H
【解析】(1)根据题目给出的流程图和信息:氮气和氢气在高温、高压、催化剂条件下生成氨气,该反应的符号表达式是:N2+3H2 ![]() 2NH3;(2)氮气和氢气可以循环利用;(3) 由表格数据可知:在1.01×105Pa时,欲将NH3与N2、H2分离,最好将温度控制在-33.35~-195.8之间;(4) 图2是合成塔中发生反应的微观粒子示意图,由图可知两种反应物N2与H2的分子个数比为1:3;该反应中的最小粒子是N、H原子.
2NH3;(2)氮气和氢气可以循环利用;(3) 由表格数据可知:在1.01×105Pa时,欲将NH3与N2、H2分离,最好将温度控制在-33.35~-195.8之间;(4) 图2是合成塔中发生反应的微观粒子示意图,由图可知两种反应物N2与H2的分子个数比为1:3;该反应中的最小粒子是N、H原子.
所以答案是:(1)N2+3H2 ![]() 2NH3;(2)N2、H2;(3) -33.35;(4) 1:3;N、H.
2NH3;(2)N2、H2;(3) -33.35;(4) 1:3;N、H.
【考点精析】通过灵活运用书写化学方程式、文字表达式、电离方程式,掌握注意:a、配平 b、条件 c、箭号即可以解答此题.

练习册系列答案
相关题目