��Ŀ����
����Ŀ��21���͵���Դ������ﮣ�Li������ﮣ�������21���͵���Դ����������ǰ�ֻ��й㷺ʹ�õĵ�أ���Ҫ�Ǹ���﮵�أ���ش��������⣺
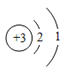
��1���ԭ�ӵ�ԭ�ӽṹʾ��ͼ��ͼ��ʾ���ԭ���ڻ�ѧ��Ӧ�����ף���õ�����ʧȥ���� ���ӱ�����ӣ������ӷ���Ϊ ��
��2���о�������﮵Ľ�����ԱȽϻ��ã�д���������ϡ���ᷴӦ�Ļ�ѧ����ʽ
��
��3������﮳�������﮵���⣬���������ڴ�����������ԭ���ǽ�����������������ɰ�ɫ��ĩ״���⻯ﮣ�LiH�����⻯���ˮ��Ӧ����������﮺�������д�����������з�����Ӧ�Ļ�ѧ����ʽ
��
���𰸡�
��1��ʧȥ Li
��2��2Li+H2SO4=Li2SO4+H2��
��3��2Li+2H2O=2LiOH+H2��
��������
�����������1�������ԭ�ӵ�ԭ�ӽṹʾ��ͼ��֪����������������4����������ʧȥ�����һ�����ӣ���һ����λ����ɣ������ӷ���Ϊ�� Li+
��2��﮵Ľ�����ԱȽϻ��ã��ʽ����������ϡ���ᷴӦ������������ѧ��Ӧ�Ļ�ѧ����ʽΪ��2Li+H2SO4=Li2SO4+H2��
��3���⻯���ˮ��Ӧ����������﮺���������Ӧ�Ļ�ѧ����ʽΪ��2Li+2H2O=2LiOH+H2��

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ