题目内容
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。请按要求完成下列问题:
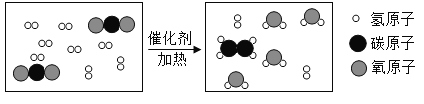
(1)A、B、C、D表示四种物质,在高温条件下,A和B反应生成C和D,微观示意图如下所示

①每个A分子是由_____________________个原子构成的。
②反应后,生成C和D两种粒子的个数比为_____________________________。
③下列结论中,正确的是____________________(填序号)。
aA物质中氢元素的质量分数为25%
b反应前后各元素化合价均没有改变
c反应前后分子的个数没有改变
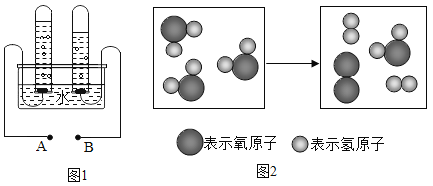
(2)如图是钠元素、氯元案在元素周期表中的信息及有关粒子的结构示意图。请回答下列问题:
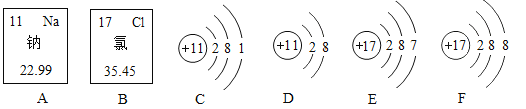
①D所表示的粒子是____________________________(填写化学符号),氯原子的结构示意图是_____ (填序号)。
②与元素的化学性质关系最密切的是____________________________(填写字母序号)。
A原子的核外电子数
B元素的相对原子质量
C原子的最外层电子数
【答案】5 1:3 a Na+ E C
【解析】
(1)根据图示的分子结构可知该反应的方程式为CH4+H2O![]() CO+3H2;
CO+3H2;
①每个A分子是由5个原子构成的。
②由方程式可以看出生成C和D两种粒子的个数比为1:3;
③a、A是CH4,其中氢元素的质量分数为![]() ×100%=25%,正确;
×100%=25%,正确;
b、根据方程式CH4+H2O![]() CO+3H2中反应前后的物质情况可知,碳和氢的化合价均发生了改变,但氧元素的化合价没有变化,b错误;
CO+3H2中反应前后的物质情况可知,碳和氢的化合价均发生了改变,但氧元素的化合价没有变化,b错误;
c、根据方程式CH4+H2O![]() CO+3H2中反应前后的分子个数情况可知,分子个数发生了改变,c错误;
CO+3H2中反应前后的分子个数情况可知,分子个数发生了改变,c错误;
故填:5;1:3;a;
(2)①D是钠原子失去1个电子后形成的钠离子,可以表示为Na+;
氯元素是17号元素,氯原子核外电子数是17个,第一层是2个,第二层是8个,第三层是7个,因此氯原子的结构示意图是E。
故填:Na+;E。
②原子最外层电子数小于4的,反应中容易失去电子,大于4的,反应中容易得到电子,因此与元素的化学性质关系最密切的是原子的最外层电子数。
故填:C。

 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】化学兴趣小组的同学学习了“二氧化锰在过氢北氯溶液分解中起催化作用”后,想探究四氧化三铁能否在过氧化氢溶液分解中起催化作用,请你一起参与他们的探究过程。
(提出问题)四氧化三铁能否作过氧化氢溶液分解的催化剂呢?
(猜想与假设)四氧化三铁能作为过氧化氢溶没分解的催化剂。
(进行试验)
实验编号 | 实验操作 | 实验现象 |
① | 在试管中加入过氧化氢溶液。然后将带火星的木条伸入试管中 | 产生少量气泡,木条不复燃 |
② | 在装有过氧化氢溶液的试管中加入1g四氧化三铁,然后将带火星的木条伸入试管中 | 产生大量气泡,木条________ |
③ | 待②中反应结束,将试管中的剩余物进行过滤,洗涤、干燥、称量 | 称得固体质量为1g |
④ | 将③中所得固体放入试管中,向其中加入过氧化氢溶液,然后将带火星的木条伸入试管中 | _________ |
(实验结论)(1)实验③④证明,四氧化三铁的____和____在反应前后均没有发生变化,可以作为过氧化氢溶液分解的催化剂。
(2)写出四氧化三铁催化过氧化氢溶液分解的化学方程式:_____________。
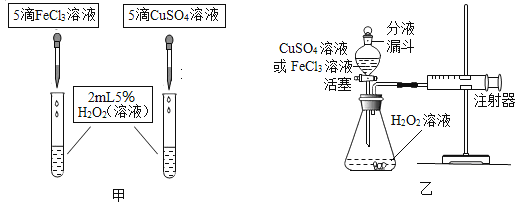
(实验拓展)小组成员小丽通过查阅资料,结合本次实验获知FeCl3溶液、CuSO4溶液都可以代替二氧化锰作H2O2分解的催化剂。于是她又设计并进行了实验来比较相同浓度的FeCl3溶液、CuSO4溶液的催化效果。
(1)若用图甲装置进行实验,应观察同时滴入两种溶液后_________来判断FeCl3溶液、CuSO4溶液的催化效果。
(2)若用图乙装置进行实验,应测试生成等体积气体时所需的__________来判断FeCl3溶液、CuSO4溶液的催化效果。