题目内容
某矿石的主要成分是一种化合物,取该矿石加入稀盐酸中,生成氯化镁、水和一种使澄清石灰水变浑浊的气体,则该矿石中含有的元素一定有
| A.碳元素、氧元素、氯元素 | B.镁元素、碳元素、氯元素 |
| C.氯元素、碳元素、氢元素 | D.镁元素、碳元素、氧元素 |
D
解析试题分析:根据质量守恒定律的实质进行分析,化学变化前后元素的种类不变;根据题意,该矿石和稀盐酸反应,生成了氯化镁、水和二氧化碳,即生成物中的元素有镁、氯、氢、氧、碳等元素,则反应物中也应含有这五种元素,由于盐酸中已能确定含有氢、氯元素,故该矿石中一定含有的元素是镁元素、碳元素、氧元素。故选D
考点:元素在化学变化过程中的特点
点评:理解和熟记质量守恒定律及其应用,是解答本题的关键;可以依据质量守恒定律的实质进行分析,即在化学变化前后,原子的种类、个数都不变,则元素的种类也不变,所以物质的总质量不变。

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
石油是一种没有固定沸点的油状物,经过汽化、冷凝分离后可得到汽油、煤油等产品。由此可以判定石油属于
| A.氧化物 | B.纯净物 | C.化合物 | D.混合物 |
下列物质属于纯净物的是( )
| A.酸牛奶 | B.干冰 | C.葡萄酒 | D.自来水 |
经测定,甲醛(CH2O)、醋酸(C2H4O2)、丙酮(C3H6O)三种物质的混合物中含氢元素8g,则该混合物完全燃烧后产生二氧化碳气体的质量是
| A.48g | B.72g | C.120g | D.176g |
下列有关分子、原子、离子的叙述错误的是( )
| A.带电的原子或原子团叫做离子 |
| B.分子是保持物质化学性质的最小粒子 |
| C.原子是不能再分的最小粒子 |
| D.原子、分子、离子都是构成物质的粒子 |
芯片是“智能家电”的核心部件,它是以高纯度单质硅为材料制成的。制取高纯硅的化学方程式为:①SiO2+2C 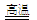 Si(粗)+2CO↑ ②Si(粗)+3HCl
Si(粗)+2CO↑ ②Si(粗)+3HCl 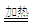 SiHCl3+H2
SiHCl3+H2
③SiHCl3+H2 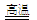 Si(纯)+3HCl。下列说法错误的是
Si(纯)+3HCl。下列说法错误的是
| A.①②③属于同一基本反应类型 | B.②③的目的是将粗硅提纯 |
| C.生产过程中HCl可以循环使用 | D.上述反应只需在干燥的设备中进行 |
根据下面微粒结构示意图给出的信息,下列说法错误的是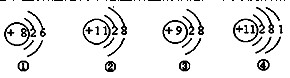
| A.①元素通常显+2价 | B.粒子②和③的化学性质相对稳定 |
| C.粒子③是阴离子 | D.粒子②和④属于同种元素 |
分子、原子、离子都是构成物质的粒子。下列说法不正确的是
| A.干冰是由二氧化碳分子构成的 |
| B.空气中既有分子构成的物质又有原子构成的物质 |
| C.氯化钠是由阴阳离子构成的 |
| D.过氧化氢是由氢气分子和氧气分子构成 |
臭氧发生器可将氧气转化为臭氧(O3)。下列说法正确的是
| A.臭氧是由三个氧原子构成的 |
| B.氧气和臭氧都是由氧元素组成的单质 |
| C.氧气与臭氧的性质相同 |
| D.氧气转化为臭氧是物理变化 |