题目内容
【题目】高纯碳酸钙广泛应用于电子、医药等领域。某化工厂利用优质石灰石(含少量SiO2等不溶于水和稀盐酸的杂质)为原料得到高纯CaCO3.其工艺流程如图:
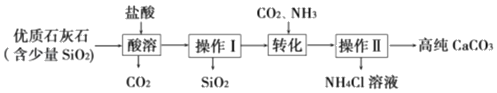
(1)该流程图中出现的氧化物有二氧化碳和_____(填名称)。
(2)实验室进行操作I的名称是_____,进行该操作时需要的玻璃仪器有烧杯、漏斗、_____。
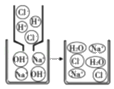
(3)请完成“转化”步骤中发生反应的化学方程式:CaCl2+_____NH3+CO2+_____═CaCO3↓+2NH4Cl
(4)该工艺的副产品NH4Cl的用途有_____(写出一种即可)。
【答案】二氧化硅(填名称) 过滤 玻璃棒 2 H2O 氮肥
【解析】
(1)氧化物是两种元素组成且其一为氧元素的化合物,所以该流程图中出现的氧化物有二氧化碳和 二氧化硅;
(2)实验室进行操作I得到不溶性物质和溶液,所以为固体和液体分离,为过滤,进行该操作时需要的玻璃仪器有烧杯、漏斗、玻璃棒;
(3)根据图中“转化”步骤中反应物为氯化钙和氨气以及二氧化碳,据质量守恒定律可知,反应前后原子的种类、个数不变,生成物氯化铵中氮原子和氢原子个数小于氨气中氮原子和氢原子个数比,所以水应该也是反应物,所以发生反应的化学方程式:CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl;
(4)该工艺的副产品NH4CI的用途有氮肥。

练习册系列答案
相关题目