题目内容
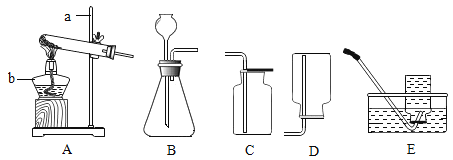
【题目】实验室制取二氧化碳气体有下列仪器供选用:

请你回答下列问题:
(1)制取二氧化碳气体所需的药品是______,写出制取反应的文字表达式_____。
(2)收集二氧化碳气体的方法是_____。
(3)制取并收集二氧化碳气体所需的仪器是(用仪器的序号回答)_____。
(4)检验二氧化碳气体是否收集满的方法是____。
(5)利用实验室里制取二氧化碳气体的发生装置,还能制取另一种气体,写出制取该气体的文字表达式____。
【答案】大理石(或石灰石)和稀盐酸 碳酸钙+稀盐酸→氯化钙+水+二氧化碳 向上排空气法 ACDE 将燃着的木条放在集气瓶口 双氧水![]() 水+氧气
水+氧气
【解析】
本题主要考察实验室制取二氧化碳的相关知识
(1)实验室常用大理石或石灰石与稀盐酸反应制取二氧化碳,其反应表达式为碳酸钙+稀盐酸→氯化钙+水+二氧化碳;
(2)二氧化碳能溶于水且密度比空气大,所以可用向上排空气法收集;
(3)收集二氧化碳要用向上排空气法,所以要选择E导管,则一定要用到D长颈漏斗,所以制取并收集二氧化碳所需的仪器为ACDF;
(4)检验二氧化碳集满的方法是将燃着的木条放在集气瓶口;
(5)实验室制取二氧化碳气体发生装置为固体和液体常温下反应,可用于双氧水制取氧气的发生装置,文字表达式为双氧水![]() 水+氧气。
水+氧气。

【题目】实验探究题
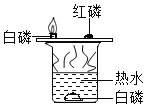
(实验回顾)18世纪末,英国科学家普利斯特里和卡文迪许把“易燃空气”与空气或氧气混合后盛在干燥、洁净的玻璃瓶中,当用电火花点火时,发出震耳的爆鸣声,且玻璃瓶内壁上出现了液滴。一年之后,拉瓦锡重复了他们的实验,并做了一个相反的实验:让水蒸气通过一根烧红的枪管,得到了“易燃空气”。这里的“易燃空气”是指_____(填化学式)
(实验重现)某化学兴趣小组的同学在创新的基础上,在实验室中重做上述两个实验,做法如下:
实验1:水的通电分解实验
如图1所示,打开活塞b,用燃着的木条在玻璃管尖嘴口检验反应产生的气体,看到的现象是_____,证明该气体为_____。写出水的通电分解反应的化学方程式_____,
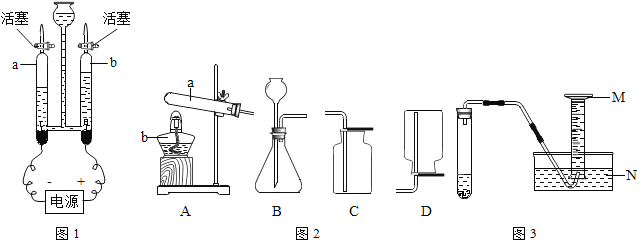
实验2:“易燃空气”与氧气混合后的点燃实验
实验室现有过氧化氢溶液、高锰酸钾、二氧化锰、稀硫酸、锌粒,图2是实验室常用部分仪器:
(1)①仪器的名称:a是_____。
②实验室制取氧气的化学方程式为_____(写一个),实验时对应的气体发生和收集装置分别是_____(填标号,下同)和_____。
(2)实验室利用锌和稀硫酸制取较多量的“易燃空气”,且可以随时补充液体,你选择的装置是_____(填序号)。
(3)验纯后用装满水的10mL量筒代替小试管收集“易燃空气”,装置如图3所示。
①10mL量筒的最大刻度靠近_____端。(填写“M”或“N”)
②当10mL量筒中的水全部被排尽后,实际收集到的“易燃空气”体积V_____10.0mL.(填写“>”、“=”或“<”)
(4)该兴趣小组的同学决定利用制得的“易燃空气”和空气继续进行探究,他们取7支试管,依次盛水90%(体积分数)、80%…再用排水集气法收集“易燃空气”,而后分别把试管口移近酒精灯的火焰,实验结果如下表所示:
分析表中信息,完成下列问题:
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
“易燃空气”体积分数(%) | 90 | 80 | 70 | 50 | 20 | 10 | 5 |
空气体积分数(%) | 10 | 20 | 30 | 50 | 80 | 90 | 95 |
点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱的爆鸣声 | 强的爆鸣声 | 强的爆鸣声 | 弱的爆鸣声 | 不燃烧 不爆鸣 |
①在混合气体爆炸范围内,“易燃空气”的体积分数约为_____;
②你对燃烧或燃烧条件的新认识是_____。
【题目】实验是科学探究的重要方法。
实验探究一:气体实验室制法
查阅资料:① 实验室用铜与浓硝酸反应制取NO2气体。
② NO2 是一种红棕色的气体,密度比空气大,能与水反应生成HNO3和NO气体,NO是一种无色气体,NO和NO2都是大气污染物。 根据图所示装置回答有关问题。
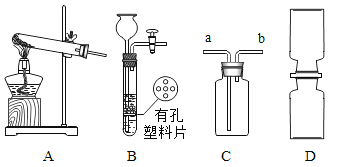
(1)实验室制取NO2气体的发生装置是_____(填装置序号),用C装置收集NO2气体时,NO2应从导管_____(填“a”或“b”)进入。
(2)NO2气体不能用排水法收集的原因(用化学方程式解释)_____。
(3)用D装置演示分子运动实验,为了缩短演示时间,应将盛有NO2的集气瓶 最好放在_____(填“上”或“下”)面,另一瓶是空气。
实验探究二:探究影响化学反应速率的因素 以过氧化氢分解为研究对象进行实验。化学小组均采用如图装置进行实验,记录收集10ml氧气的时间。

实验室提供的试剂:2.5%、5%、10%三种 浓度的H2O2溶液;MnO2;CuO;红砖粉末。 数据记录如下:
实验序号 | H2O2 溶液 | 其他物质质量 | 收集 10ml氧气的时间/s |
① | 5ml10% | 0.5g MnO2 | 10 |
② | 5ml10% | 0.5g 红砖粉末 | 60 |
③ | 5ml10% | 0.5g CuO | 20 |
④ | 5ml5% | 0.5g MnO2 | 15 |
(1)小明通过分析实验①②③的数据。
得出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用。
小洪同学对该结论提出疑问,并补充对比实验,其实验操作为:____。 结果:长时间(大于 100s)后,收集到很少量气体。 结论:红砖粉末_____(选填“有”、“无”)催化作用,三者中_____催化效率最高。 写出实验③的反应化学方程式:_________。
(2)小王同学通过分析实验_____(填实验序号)。 得出结论为:当__________时,反应物浓度越大,反应速率越快。
(3)影响化学反应速率的因素还有____________________________。
实验探究三:二氧化碳气体与氢氧化钠溶液的反应情况。
化学小组用小烧杯盛装一定量的氢氧化钠溶液并通入一定量的CO2气体进行探究。
(提出问题)
氢氧化钠溶液中通入/span>CO2一段时间后所得的溶液(下面称样品)中会有什么溶质?
(查阅资料)
① 通入少量的二氧化碳时,NaOH与CO2反应的化学方程式_____。
② 通入过量的二氧化碳时,反应的化学方程式为Na2CO3+CO2+H2O= 2NaHCO3
③ 碳酸氢盐都能溶于水,BaCO3难溶于水且是白色固体。
④ Na2CO3、NaHCO3的溶液呈碱性、BaCl2 呈中性
(提出猜想)A.溶质是NaOH、Na2CO3; B.溶质是Na2CO3;C.溶质是Na2CO3、NaHCO3; D.溶质是NaHCO3
(设计实验方案)
实验步骤 | 实验现象 | 实验结论 |
取少量样品于试管中, 滴加几滴_______试液(填酸碱指示剂) | 溶液变红色 | 该溶液显碱性 |
②另取少量样品于试管中, 滴加过量的 BaCl2溶液 | 有白色沉淀生成 | 猜想_____不成立 |
③取步骤②静置后的上层清液,滴入稀盐酸 | 有气泡冒出 | 猜想A和B不成立 |
(得出结论)猜想_____成立
(讨论交流)
(1)同学们讨论后一致认为实验步骤①是多余的。 理由是:_____。
(2)若长时间向澄清石灰水中通入二氧化碳会看到什么样的现象呢? 现象是:_____。