题目内容
【题目】控制化学反应的条件可以促进或抑制化学反应,更好使化学反应为人类造福.
(1)如图是科学家正在研究的二氧化碳循环利用技术: 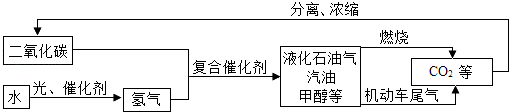
①二氧化碳与氢气在催化剂、高温条件下.生成甲醇(CH4O)和水,写出该反应的文字表达式 , 甲醇中碳元素的化合价为 .
②从图中分析得出的下列结论中,正确的是(填序号)
A.该技术符合低碳经济的理念
B.水生成氢气的过程中所用的催化剂一定是二氧化锰
C.该技术有助于缓解全球面临的能源危机
D.液化石油气、汽油、甲醇均为纯净物
(2)水在光、催化剂作用下生成氢气和氧气,该反应的基本反应类型为 .
(3)汽油燃烧时氧气浓度越大,燃烧越剧烈,试从微观角度解释这是因为 .
【答案】
(1)二氧化碳+氢气 ![]() 甲醇+水;-2;AC
甲醇+水;-2;AC
(2)分解反应
(3)氧气浓度越大,一定体积内氧分子数目越多,氧气分子与汽油分子碰撞的次数越多,燃烧越剧烈
【解析】解:(1)①二氧化碳和氢气生成甲醇(CH3OH)和水,文字表达式为:二氧化碳+氢气 ![]() 甲醇+水;设甲醇中碳元素的化合价为x,则x+1×3﹣2+1=o,x=﹣2;②A、二氧化碳循环利用,符合低碳经济的理念,故对;B、水生成氢气的过程中所用的催化剂不一定是二氧化锰,故错;C、二氧化碳循环利用,该技术有助于缓解全球面临的能源危机,故对;D、液化石油气、汽油、甲醇等物质中共含有碳、氢、氧三种元素,故错;(2)水在光、催化剂作用下生成氢气和氧气,该反应的基本反应类型为分解反应;(3)氧气浓度越大,一定体积内氧分子数目越多,氧气分子与汽油分子碰撞的次数越多,燃烧越剧烈;所以答案是:(1)①二氧化碳+氢气
甲醇+水;设甲醇中碳元素的化合价为x,则x+1×3﹣2+1=o,x=﹣2;②A、二氧化碳循环利用,符合低碳经济的理念,故对;B、水生成氢气的过程中所用的催化剂不一定是二氧化锰,故错;C、二氧化碳循环利用,该技术有助于缓解全球面临的能源危机,故对;D、液化石油气、汽油、甲醇等物质中共含有碳、氢、氧三种元素,故错;(2)水在光、催化剂作用下生成氢气和氧气,该反应的基本反应类型为分解反应;(3)氧气浓度越大,一定体积内氧分子数目越多,氧气分子与汽油分子碰撞的次数越多,燃烧越剧烈;所以答案是:(1)①二氧化碳+氢气 ![]() 甲醇+水.②AC.(2)分解反应;(3)氧气浓度越大,一定体积内氧分子数目越多,氧气分子与汽油分子碰撞的次数越多,燃烧越剧烈.
甲醇+水.②AC.(2)分解反应;(3)氧气浓度越大,一定体积内氧分子数目越多,氧气分子与汽油分子碰撞的次数越多,燃烧越剧烈.
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号.

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案