题目内容
如图中的①、②是氟元素、钙元素在元素周期表中的信息,A.B.C.D是四种粒子的结构示意图.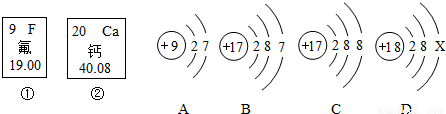
请你回答:
(1)氟元素的相对原子质量为______,钙元素的原子序数为______;
(2)若D为原子,X=______;
(3)A.B.C.D属于同种元素的粒子是______(填序号);
(4)A粒子的化学性质与B.C.D中哪一种粒子的化学性质相似______(填序号);
(5)2008年5月,我省某地发生了氢氟酸(HF)泄漏,消防队员用熟石灰对泄漏点进行处理,生成物氟化钙是不溶于水的沉淀物.请写出化学方程式______.
【答案】分析:1)根据氟元素、钙元素在元素周期表中的信息进行解答;
(2)根据在原子中,原子序数=质子数=核外电子数=核电荷数,进行解答;
(3)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,不同种元素之间的本质区别是质子数不同,进行判断解答;
(4)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,进行解答;
(5)根据书写化学方程式的要求:写,配,注,等,写出反应方程式..
解答:解:(1)根据氟元素、钙元素在元素周期表中的信息可知:氟元素的相对原子质量为 19.00;,钙元素的原子序数为:20;
故答案为;19.00; 20;
(2)根据在原子中,原子序数=质子数=核外电子数=核电荷数,则有:2+8+x=18,所以x=8,
故答案为:8;
(3)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,不同种元素之间的本质区别是质子数不同,微粒BC的质子数相同,为同种元素,
故答案为:BC;
(4)根据元素的最外层电子数相同的元素化学性质相似,微粒A与B的最外层电子数相同;
故答案为:B;
(5)根据氢氟酸(HF)泄漏用熟石灰进行处理,则反应方程式为:Ca(OH)2+2HF=CaF2↓+2H2O;
故答案为:Ca(OH)2+2HF=CaF2↓+2H2O.
点评:本题考查学生对在原子中,原子序数,质子数,核外电子数,核电荷数之间的关系及元素的最外层电子数决定元素的化学性质的理解与掌握,并注意书写化学方程式的要求
(2)根据在原子中,原子序数=质子数=核外电子数=核电荷数,进行解答;
(3)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,不同种元素之间的本质区别是质子数不同,进行判断解答;
(4)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,进行解答;
(5)根据书写化学方程式的要求:写,配,注,等,写出反应方程式..
解答:解:(1)根据氟元素、钙元素在元素周期表中的信息可知:氟元素的相对原子质量为 19.00;,钙元素的原子序数为:20;
故答案为;19.00; 20;
(2)根据在原子中,原子序数=质子数=核外电子数=核电荷数,则有:2+8+x=18,所以x=8,
故答案为:8;
(3)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,不同种元素之间的本质区别是质子数不同,微粒BC的质子数相同,为同种元素,
故答案为:BC;
(4)根据元素的最外层电子数相同的元素化学性质相似,微粒A与B的最外层电子数相同;
故答案为:B;
(5)根据氢氟酸(HF)泄漏用熟石灰进行处理,则反应方程式为:Ca(OH)2+2HF=CaF2↓+2H2O;
故答案为:Ca(OH)2+2HF=CaF2↓+2H2O.
点评:本题考查学生对在原子中,原子序数,质子数,核外电子数,核电荷数之间的关系及元素的最外层电子数决定元素的化学性质的理解与掌握,并注意书写化学方程式的要求

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



