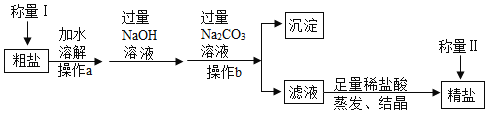
题目内容
【题目】某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如下图所示的实验。
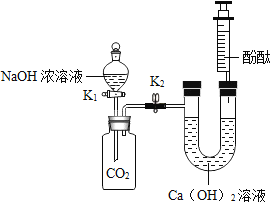
(1)将足量的氢氧化钠浓溶液装入分液漏斗中,先打开阀门K1,广口瓶中发生反应的化学方程式为____,待氢氧化钠溶液完全进入广口瓶之后立即关闭K1,充分反应后,打开止水夹K2,观察到的现象是___。
(2)同学们将实验后的废液倒入烧杯中并过滤,取滤液于试管中加入足量的稀盐酸,无气泡产生,说明废液中的溶质为_____________(写出所有可能)。
【答案】2NaOH+CO2=Na2CO3+H2O U型管中的溶液有部分沿导管进入广口瓶,广口瓶中出现浑浊,注射器中的液体自动喷入U型管,且变为红色 NaOH或NaOH和Ca(OH)2
【解析】
(1)打开阀门K1后,氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,据此写出反应的化学方程式;关闭K1,充分反应后打开止水夹K2,由于二氧化碳与氢氧化钠反应,瓶内压强减小,导致U型管中的溶液有部分沿导管进入广口瓶,广口瓶中出现浑浊,注射器中的液体自动喷入U型管,且U形管中溶液变为红色;
(2)滤液于试管中加入足量的稀盐酸,无气泡产生,说明溶质中不含碳酸钠,应该含有氢氧化钠或氢氧化钠和氢氧化钙的混合物。
(1)二氧化碳可以和氢氧化钠溶液反应生成碳酸钠和水,该反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;待氢氧化钠溶液完全进入广口瓶之后立即关闭K1,充分反应后,打开止水夹K2,由于二氧化碳与氢氧化钠反应,集气瓶中气体体积减小,则瓶内压强减小,导致U型管中的溶液有部分沿导管进入广口瓶,广口瓶中氢氧化钙溶液和碳酸钠溶液反应生成碳酸钙沉淀,溶液变浑浊,注射器中的液体自动喷入U型管,酚酞遇到U形管中的氢氧化钙溶液变为红色。
故填:2NaOH+CO2=Na2CO3+H2O;U型管中的溶液有部分沿导管进入广口瓶,广口瓶中出现浑浊,注射器中的液体自动喷入U型管,且变为红色。
(2)将实验后的废液倒入烧杯中并过滤,取滤液于试管中加入足量的稀盐酸,无气泡产生,说明滤液中不含碳酸钠,因为碳酸钠会与稀盐酸反应生成二氧化碳气体;由于氢氧化钙溶液和碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,所以反应后的废液中一定含有NaOH,可能含有氢氧化钙,因为氢氧化钙可能过量也可能恰好与碳酸钠完全反应。故答案为:NaOH或NaOH和Ca(OH)2。

【题目】某校化学兴趣小组在查阅资料时发现:可燃物燃烧需要的最低氧含量数据如下表。
可燃物名称 | 蜡烛 | 木炭 | 棉花 | 红磷 | 白磷 |
最低氧含量/% | 16 | 14 | 8 | 8.8 | 3.2 |
请结合数据回答下列问题:
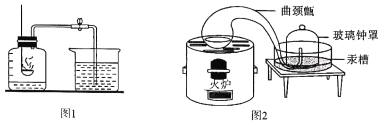
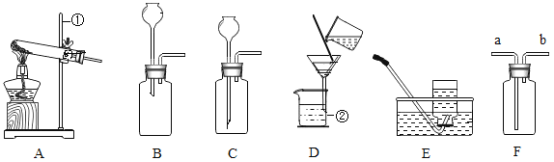
(1)图1为教材中测量空气中氧气体积分数的实验装置图,请写出集气瓶中发生的化学反应程式:___________。结合数据,你认为红磷适合于测量空气中氧气的体积分数吗?并说明你的理由:_________。但实验过程中又确实看到进来的水的体积约占集气瓶内容积的1/5,其原因可能是________。
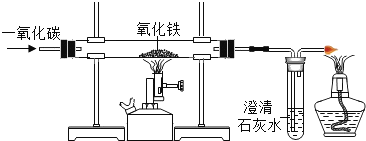
(2)图2是拉瓦锡的实验装置,回看拉瓦锡的实验,选择汞的优点有_________(填序号,多选)。
A 实验过程没有污染
B 生成的化合物加热分解后又得到汞和氧气
C 在汞槽中起到液封作用
D 能将密闭装置内空气中的氧气几乎耗尽
【题目】某小组同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行探究。
【提出问题】①三种溶液的酸碱性?
②它们与酸反应时溶液的pH如何变化?
【查阅资料】
pH | 2~3 | 4~6 | 7 | 8~9 | 10~11 | 12~14 |
紫甘蓝汁液显示的颜色 | 紫红 | 浅紫 | 紫色 | 蓝色 | 绿色 | 黄色 |
【实验1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 紫色 | 蓝色 | 绿色 | 黄色 |
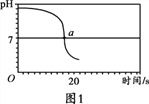
【实验2】向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图1所示。
【实验3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图2、图3所示。将图2与图3的阴影部分进行叠加,发现两者基本重合。

【解释与结论】
(1)实验1得出三种溶液的碱性由强到弱的顺序为________________。
(2)实验2证明了氢氧化钠能与盐酸发生反应,其理由是_________,实验结束,向反应后的溶液中滴加紫甘蓝汁液,观察到的现象是_________。
(3)实验3中,b点的溶质为_________,c点后发生反应的化学方程式为_________。
(4)依据实验3获取的信息,鉴别Na2CO3和NaHCO3固体的实验方案为_________。