题目内容
【题目】通过海水晾晒可得粗盐。粗盐除 NaCl 外,还含有 MgCl2、CaCl2 以及泥沙 等杂质。为了有效将粗盐提纯,实验的各步操作流程如下图所示。
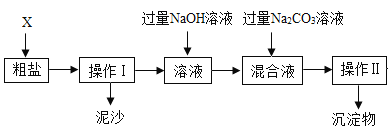
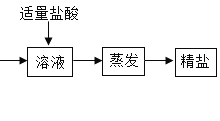
根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的 X 物质是____________。
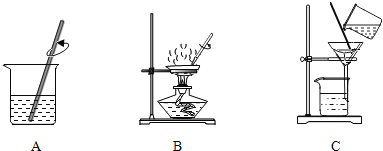
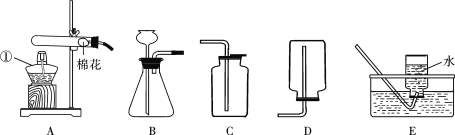
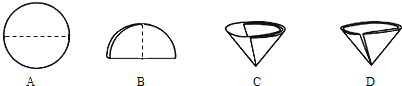
(2)操作Ⅰ和操作Ⅱ的名称是_______。该操作中需要将圆形滤纸折叠处理,下列图 示中不该出现的情形是_______________(填序号) 。
(3) 在 实 验 过 程 中 加 入 过 量 的 NaOH 溶液的 有 关 化 学 方 程 式 是___________________。
(4)在蒸发操作中用玻璃棒的作用是______________。
(5)下列有关蒸发结晶操作描述正确的是____________。
A 当加热至有晶体析出时,即停止加热
B 当蒸发皿中出现较多固体时,即停止加热
C 当水分完全蒸干时,即停止加热
D 蒸发皿应放在石棉网上加热,放止破损
(6)加入盐酸的目的是_______________,判断加入的盐酸“适量”的方法是___________。
(7)实验所得精盐的质量________________(填“大于”、“小于”或“等于”)粗盐中 NaCl 的质 量。
【答案】水 过滤 D ![]() 搅拌,防止局部温度过高液体飞溅。 B 去除过量的氢氧化钠碳酸钠 加盐酸至不再产生气泡为止 大于
搅拌,防止局部温度过高液体飞溅。 B 去除过量的氢氧化钠碳酸钠 加盐酸至不再产生气泡为止 大于
【解析】
本题考察粗盐的提纯属于除杂类型的题,对于除杂的原则:
不增:不引入新杂质
不减:被提纯物质不能减少
易分离:杂质要容易分离
易复原:被提纯后被提纯物质要恢复原来的状态。
(1)难溶性杂质的去除通过溶解过滤的方法,溶解的时候需要要加水,故填:水。
(2)操作Ⅰ和操作Ⅱ都是固液分离的操作是过滤,故填:过滤;
下图中不该出现的情形是D,否则滤液没有经过滤纸,仍然浑浊,故填:D。
(3)加入过量氢氧化钠是为了去除氯化镁,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,反应的化学方程式为:
![]()
故填:![]()
(4)蒸发过程中容易造成局部温度过高液体飞溅为尽量减少飞溅,用玻璃棒连续搅拌,故填:搅拌,防止局部温度过高液体飞溅。
(5)蒸发操作蒸发到蒸发皿出现较多固体时停止加热:
A 当加热至有晶体析出时,即停止加热,水分不能完全蒸干,不符合题意;
B 当蒸发皿中出现较多固体时,即停止加热,利用余热使水分蒸干,符合题意;
C 当水分完全蒸干时,即停止加热,会使食盐烧焦,不符合题意;
D 蒸发皿应放在石棉网上加热,放止破损,蒸发皿可以直接加热不需要放到石棉网上加热,不符合题意,故选B。
(6)盐酸可以和氢氧化钠和碳酸钠都反应,去除过量的氢氧化钠和碳酸钠,
故填:去除过量的氢氧化钠碳酸钠;
盐酸和碳酸钠反应会产生氯化钠、二氧化碳和水,当加入盐酸不再产生气泡时,所加盐酸适量,故填:加盐酸至不再产生气泡为止。
(7)除杂的过程当中杂质和加入物质反应会生成氯化钠,氯化钠最多,故填:大于。

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案