题目内容
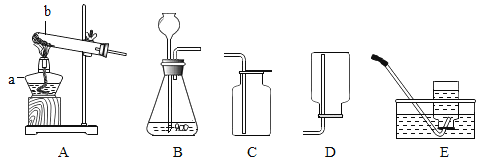
【题目】某补钙剂的主要成分是碳酸钙,欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图 1 的操作,所加稀盐酸的质量与生成气体的质量关系如图 2 所示。(已知:其他成分不参与反应)
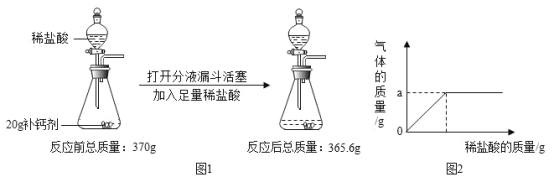
(1)图 2 坐标中 a 的数值为 ;实验中,装置的气密性对测定结果 (选填“有”或“无”)影响。
(2)实验中,要用溶质质量分数为 36.5%的浓盐酸,配制 100g 溶质质量分数为14.6%的稀盐酸,配制过程中需要加入水的质量为 。
(3)计算该补钙剂中碳酸钙的质量分数。(根据化学方程式计算,写出完整步骤)
【答案】(1) 4.4 ;无(2)60g(3)50%
【解析】
解:(1)完全反应后,质量的减少量即为生成二氧化碳的质量。由质量守恒定律可知,生成二氧化碳的质量为:370g-365.6g=4.4g,由于是让生成的二氧化碳跑掉,借助质量变化求算生成的二氧化碳的质量,该实验中,装置的气密性对测定结果无影响。
(2)设配制100g14.6%的稀盐酸加入水的质量是为![]() ,则根据稀释前后溶质的质量不变可得:100g×14.6%=(100g-
,则根据稀释前后溶质的质量不变可得:100g×14.6%=(100g-![]() )×36.5%,解得
)×36.5%,解得![]() =60g;
=60g;
(3)设该补钙剂中碳酸钙的质量分数为![]() ,
,
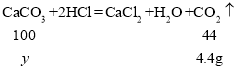
![]()
![]() 10g
10g
补钙剂中CaCO3的质量分数为 ![]() 100% 50% 。
100% 50% 。
答:该补钙剂中CaCO3的质量分数为50% 。

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目