题目内容
【题目】草木灰是农家肥料,它的主要成分是碳酸钾。某化学兴趣小组取100g草木灰于烧杯中,不断滴入稀盐酸溶液,当滴入50g稀盐酸时,恰好不再有气泡产生,此时烧杯中的残余混合物质量为147.8g。碳酸钾与盐酸反应的化学方程式为K2CO3+2HCl=2KCl+H2O+CO2↑(假设草木灰的其他成分不与酸反应),请计算:
(1)生成物中水的化学式量___________。
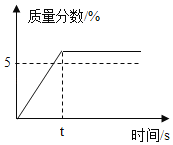
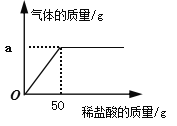
(2)下图表示反应过程放出的气体质量与加入盐酸的关系曲线,则图中纵坐标上a点数值为:a=_________g;
(3)稀盐酸中溶质的质量分数(请写出计算过程)。________
【答案】18 2.2 7.3%
【解析】
(1)水的化学式量=1![]() 2+16=18;
2+16=18;
(2)质量守恒定律可知,二氧化碳的质量为100g+50g-147.8g=2.2g;
(3)设稀盐酸中溶质的质量分数为x,

![]() ,
,
x=7.3%。

练习册系列答案
相关题目