题目内容
【题目】小金做了如下实验:将4.2克铁粉和4.0克氧化铜粉末均匀混合,然后一次性投入盛有200克9.8%稀硫酸的大烧杯中。观察到如下现象:立即出现红色固体,前阶段没有明显的气泡产生,后阶段产生大量无色气泡,充分反应后上层清液是浅绿色。由此小金作出下列判断,其中不合理的是
A. “立即出现红色固体”是由于很快发生了如下转化:CuO![]() CuSO4
CuSO4![]() Cu
Cu
B. “产生大量无色气泡”是由于发生了如下反应:Fe+H2SO4=FeSO4+H2↑
C. 该实验条件下,硫酸铜比稀硫酸更容易跟铁粉发生反应
D. 在不同浓度的硫酸铜和稀疏酸的混合溶液中投入铁粉,都是硫酸铜先跟铁粉反应
【答案】D
【解析】A、“立即出现红色固体”是由于很快发生了如下转化:CuO![]() CuSO4
CuSO4![]() Cu,铜是红色,故A正确;B、“产生大量无色气泡”是由于发生了如下反应:Fe+H2SO4=FeSO4+H2↑,故B正确;C、该实验条件下,硫酸铜比稀硫酸更容易跟铁粉发生反应,故C正确;D、在不同浓度的硫酸铜和稀疏酸的混合溶液中投入铁粉,不一定都是硫酸铜先跟铁粉反应,故D错误。
Cu,铜是红色,故A正确;B、“产生大量无色气泡”是由于发生了如下反应:Fe+H2SO4=FeSO4+H2↑,故B正确;C、该实验条件下,硫酸铜比稀硫酸更容易跟铁粉发生反应,故C正确;D、在不同浓度的硫酸铜和稀疏酸的混合溶液中投入铁粉,不一定都是硫酸铜先跟铁粉反应,故D错误。

【题目】控制变量,设计对比实验是实验探究的重要方法。
实验一:区分硬水和软水。
| 本实验条件除了要控制所取硬、软水的体积相同外,还必须要控制___________相同。 |
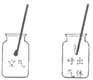
实验二:探究人体吸入的空气与呼出的气体有什么不同。
| 将燃着的小木条分别插入空气样品和呼出气体的样品中,对比观察到的现象,可以得出的结论是___________。 |
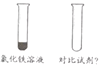
实验三:探究决定氯化铁溶液颜色的粒子。
| 氯化铁溶液呈黄色。为了探究溶液中的哪种粒子使溶液呈黄色,小艳同学分析溶液中存在的粒子,选择了一种试剂作对比,确定了决定氯化铁溶液颜色粒子,用作对比的试剂可以是___________溶液。 |
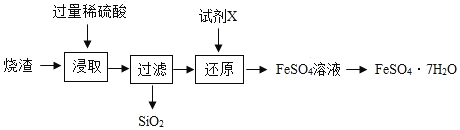
【题目】为探究盐酸的化学性质,某化学小组做了如下实验:
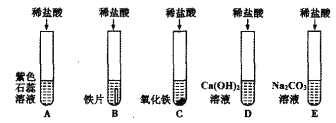
(1)A试管中的实验现象为______________,C试管中所发生反应的化学方程式为____________。
(2)将反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
(提出问题)滤液中溶质的成分是什么?
(作出猜想)猜想:NaCl
猜想二:NaCl和CaCl2
猜想三:______________
猜想四:NaCl、Ca(OH)2和HCl
(设计实验)请完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量的碳酸钠溶液。 | _________ | 猜想二不成立 |
取少量滤液于试管中, 滴加_______(填名称)。 | _________ | 猜想三成立 |
(迁移拓展)稀盐酸、稀硫酸有一些相似的化学性质,是因为在不同的酸溶液中都含有__________。