题目内容
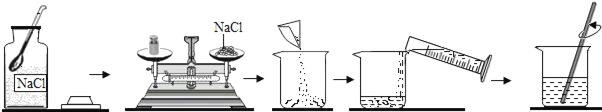
【题目】有一包白色粉末可能由NaCl、NaNO3、MgCl2、CuSO4中的一种或多种物质组成。小明为了探究其成分,设计并完成了如下图所示的实验。
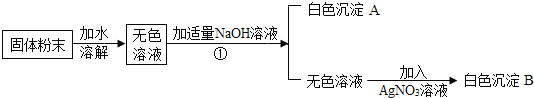
根据以上实验,回答:
(1)操作①是___
(2)原固体粉末中一定没有的成分是_______。
(3)生成沉淀A的化学方程式是 ____ 。
(4)上述实验 ____(填‘能’或‘不能’)确定原固体粉末中含有NaCl、NaNO3。
【答案】过滤 CuSO4 2NaOH+ MgCl2== Mg(OH)2↓+2NaCl 不能
【解析】
硫酸铜溶液为蓝色,一包白色粉末可能由NaCl、NaNO3、MgCl2、CuSO4、中的一种或多种物质组成,固体粉末溶解后溶液为无色,说明没有硫酸铜;溶液中加入氢氧化钠,生成白色沉淀,说明有氯化镁,因氯化镁和氢氧化钠生成氯化钠和氢氧化镁沉淀;向所得溶液中加入硝酸银生成白色沉淀,说明溶液中有氯离子,但由于氯化镁中有氯离子,因此不能证明原粉末中有氯化钠。故:
操作①是过滤,目的是将沉淀与溶液分离;
原固体粉末中一定没有的成分是硫酸铜;
生成沉淀A的化学方程式是 2NaOH+ MgCl2== Mg(OH)2↓+2NaCl;
根据上述实验不能确定原固体粉末中含有NaCl、NaNO3。

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目