题目内容
【题目】取10g某锌样品(含少量杂质,且杂质不溶于水,也不与酸反应)于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7g时,恰好完全反应,生成气体的质量与反应时间的关系如下图所示,试回答下列问题:

(1)恰好完全反应时所生成氢气的质量为_________g。
(2)样品中锌的质量分数?_______
(3)反应后,所得溶液中硫酸锌的质量分数为多少?_____
【答案】0.2 65% 16.1%
【解析】
(1)由图可知,恰好完全反应时所生成氢气的质量为0.2g;
(2)设样品中锌的质量为x,反应后生成硫酸锌的质量为y
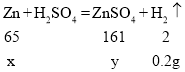
![]()
![]()
x=6.5g y=16.1g
样品中锌的质量分数为:
![]() ;
;
(3)反应后所得溶液中硫酸锌的质量分数为:
![]()
答:样品中锌的质量分数为65%,反应后所得溶液中硫酸锌的质量分数为16.1%。

【题目】课本第二单元课后作业中有“寻找新的催化剂”的探究内容,某中学探究小组据此设计了如下探究方案。
(提出问题)
红砖粉末能否作为过氧化氢分解的催化剂如果能,效果如何?
(实验探究)
实验步骤 | 实验现象 |
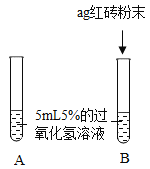
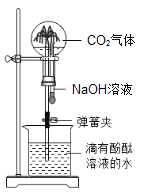
I.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向B试管中加入ag红砖粉末(如图所示)。然后分别在A、 B两支试管中插入带火星的小木条,观察现象
| A试管中无明显现象, B试管中产生气泡,带火星的小木条复燃 |
Ⅱ.待B试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星的小木条均复燃 |
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量。 | 所得固体质量仍为ag |
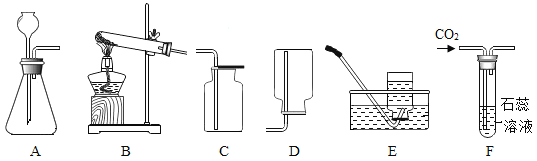
Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag红砖粉末,向D试管中加入ag二氧化锰粉末,观察现象。
| 两试管中均产生气泡且 |
(实验结论)
(1)实验I得出的结论是________。
(2)实验Ⅱ、Ⅲ证明:红砖粉末的______和_______在反应前后均没有发生变化。
(3)通过实验I-Ⅲ,可以得出的结论是__________。
(4)过氧化氢在红砖粉末催化条件下分解放出O2的化学方程式_______。
(实验评价)
(5)设计实验IV的目的是__________。
(6)若通过实验Ⅳ得出结论:红砖粉末的催化效果没有二氧化锰粉末好,那么实验Ⅳ中可以观察到的现象是:两试管中均产生气泡,且________。
(实验拓展)
査阅资料得知:氧化铜、硫酸铜溶液、猪肝、马铃薯、水泥块等也能作过氧化氢分解的催化剂。若用水泥块作为过氧化氢分解的催化剂,可以通过改变水泥块的_______提高反应速率。
【题目】小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了解铬与铝、铜的金属活动性相对强弱关系,进行如下探究活动:
(查阅资料)
(1)铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
(3)铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液。
(实验过程)取大小相同的三种金属薄片,用砂纸打磨光亮。
实验一 | 实验二 | 实验三 | |
实验方案 |
|
|
|
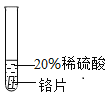
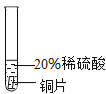
实验现象 | 铬片表面产生气泡缓慢,溶液变蓝色。 | a | 铝片表面产生气泡较快。 |
结论 | 铬能和稀硫酸发生反应,反应速率较慢。 | 铜不与稀硫酸反应 | b |
三种金属的金属活动性由强到弱的顺序是:c | |||
(回答问题)
(1)上表空白处,请填写合适内容:a_____ b_____ c_____
(2)用砂纸打磨金属片的目的是:_____。
(3)实验一中,发生反应的化学方程式是:_____。
(4)小东提出,用硫酸铜溶液代替上述实验中的稀硫酸,也能得出三种金属的相对强弱关系。小燕认为不可行,理由是_____。
(5)小清认为,只要选用三种试剂或药品,两两反应进行实验,就可以比较得出三种金属的强弱关系,这三种药品可以是_____ (写出一组即可)。