题目内容
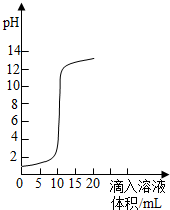 如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH
(2)根据曲线判断,该反应是将
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为
考点:中和反应及其应用,酸碱指示剂及其性质,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:(1)强酸强碱恰好中和时,溶液显中性;
(2)当溶液的pH<7时,溶液显酸性,当溶液的pH>7时,溶液显碱性,当溶液的pH=7时,溶液显中性;
(3)根据盐酸和氢氧化钠的反应原理以及图象数据来回答.
(2)当溶液的pH<7时,溶液显酸性,当溶液的pH>7时,溶液显碱性,当溶液的pH=7时,溶液显中性;
(3)根据盐酸和氢氧化钠的反应原理以及图象数据来回答.
解答:解:(1)氢氧化钠和盐酸恰好完全反应时,氢离子和氢氧根离子均无剩余,溶液显中性,pH=7,故答案为:等于;
(2)根据图象,在反应未进行时,溶液的pH=1,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入盐酸中,故答案为:氢氧化钠溶液;盐酸;(3)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为5mL时,溶液仍为强酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸,酸使石蕊显红色,故答案为:NaCl、HCl;红.
(2)根据图象,在反应未进行时,溶液的pH=1,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入盐酸中,故答案为:氢氧化钠溶液;盐酸;(3)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为5mL时,溶液仍为强酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸,酸使石蕊显红色,故答案为:NaCl、HCl;红.
点评:本题是利用酸碱中和反应结合图象知识来考查,难度较大,考查的知识面较广,要求在理解中和反应的基础上,能对反应的程度结合溶液的pH进行分析.

练习册系列答案
相关题目
通过下列实验,可以得出的相应结论正确的是( )
A、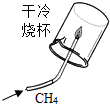 此图既说明甲烷具有可燃性,又说明甲烷是由氢元素和碳元素组成 |
B、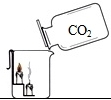 此图既说明二氧化碳的密度比空气大,又说明二氧化碳不能燃烧也不支持燃烧 |
C、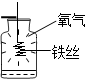 此图既说明铁具有可燃性,又说明增大氧气的浓度能促进燃烧 |
D、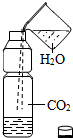 此图既说明二氧化碳可溶于水,又说明二氧化碳能与水反应 |
通过控制反应条件可以控制化学反应的快慢,下列做法是为了使化学反应变慢的是( )
| A、实验室制CO2时用块状大理石而不用碳酸钙粉末 |
| B、在煤屑中加入黄泥制成蜂窝煤燃烧 |
| C、面团发酵放在温热处 |
| D、将木炭放入纯氧气中燃烧 |