��Ŀ����
����Ŀ���Ȼ�����һ����Ҫ�����Σ��㷺������ֽ��ӡȾ����Ⱦ������
�������Ʊ���ij��ȤС��ͬѧ���ҵ��Ի�������Ҫ�ɷ��Ƕ�����������ѧʽΪFeS2��Ϊ��Ҫԭ���Ʊ��Ȼ�������Ĺ�ҵ�������̣�
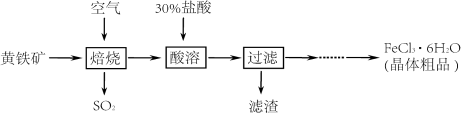
��1���������� ����������ϡ��������ж�����������Ԫ�صĻ��ϼ�Ϊ ��
��2�����չ�����Ҫ�������»�ѧ��Ӧ����ƽ��ѧ����ʽ�� FeS2 + O2 ����Fe2O3 + SO2
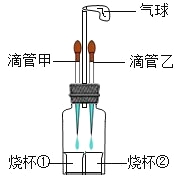
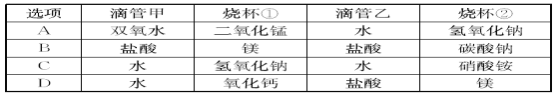
��3���ù��̲�����β���к���HCl�����壬���� ��Һ�����գ��ѧʽ����
�������ⶨ�������������в�����SO2��������ڹ�ҵ���������ᣬ����ȤС���ͬѧΪ�ⶨij����������Ԫ�صĺ������������µ�ʵ��̽����
��֪�����������������Ʒ�Ӧ���ɵ����������ܱ��������������������ơ�������ÿ����Ӧ����ȫ��������װ����ԭ�п����Բⶨ�����Ӱ�죩
�ס��Ҷ���ʵ��С������������װ�ã���ȡ��m1 g��������Ʒ������Ʒ��������ͼ��ʾ��Ӳ�ʴֲ������У���a�����ϵػ���ͨ��������������ղ������еĻ�������Ʒ����Ӧ��ȫ��

����ͬѧ������������ʵ������Ҫ�����װ������������˲ⶨ��
����ͬѧ����������Ӧ������Cƿ�е���Һ����������ͼ������
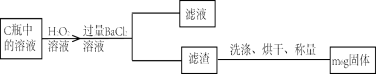
�������ۣ�
��4������װ����Aƿ����ʢ���Լ������ ��Һ���������� ��
A��Bװ���ܷ�Ե�λ�ã� ����ܡ���
��5���������Cƿ��Cƿ�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��6������ͬѧӦ������������ �����ţ���
�ٷ�ӦǰCװ�ü���������������m2 g
�ڷ�ӦǰC��Dװ�ü���������������m3 g
�۷�Ӧ��Cװ�ü���������������m4 g
�ܷ�Ӧ��C��Dװ�ü���������������m5 g
��7�����ݣ�6������ѡ���ݣ�����ͬѧ��õĸû���������Ԫ�ص����������ı���ʽΪ ��
��8������ͬѧ���յõ��Ĺ���Ļ�ѧʽΪ ����������BaCl2��Һ�Ƿ�����ķ����� �������ʵ�������ϴ��������Ŀ���� ����δϴ�Ӿ�ֱ�Ӻ�ɳ��������ʹ�ⶨ��� ���ƫ��ƫС�䡱�������������Ƿ�ϴ�������Լ��� ��Һ����С��ⶨ����Ԫ�ص����������ı���ʽΪ ��
���𰸡���1����� +2
��2��4 11 2 8 (��1��)
��3��NaOH��
��4��NaOH ���տ����е�CO2 ��
��5��SO2 + 2 NaOH = Na2SO3 + H2O
��6���ڢ�
��7����m5-m3��/2m1
��8��BaSO4 ���ã����ϲ���Һ�ټ�BaCl2��Һ�����������������ѹ���
��ȥ��������Ŀ��������� ƫ�� AgNO3 /̼����/�����Ƶ� ; 32 m6/233 m1
��������
�����������1���������ǻ������ݻ������и�Ԫ���������ϼ۴�����Ϊ0����֪���Ļ��ϼ�Ϊ+2����2�����ݻ�ѧ��Ӧǰ���ԭ�������ԭ�Ӹ������������ƽ����3��HClΪ�������壬���ü���Һ�����գ�4������������Һ��������еĶ�����̼������Ӧ��AB���ܻ������������ܳ�ȥ�����еĶ�����̼��ˮ����Ժ�ߵ�ʵ����ɸ��ţ���5������������������Ʒ�Ӧ�������������ƺ�ˮ����6��C��Dװ�������ӵ������Ƿ�Ӧ�����ɵĶ��������������֪���˶���������������ٽ����Ʒ���������ɼ������Ԫ��������������ѡ�ڢ� ����7��������������Ԫ����������Ϊ50%�����Ը��ݣ�6������ѡ���ݿɼ������Ʒ����Ԫ��������������8������������к�ǿ�������ԣ����������������������ƣ������ƺ��Ȼ����������ᱵ��������������ͬѧ���յõ��Ĺ���Ϊ���ᱵ�����������Ȼ����Ƿ�����ķ�����ȡ�ϲ���Һ�ټ��Ȼ��������а�ɫ��������֤���Ѿ������������ʵ�������ϴ��������Ŀ���dz�ȥ��������Ŀ��������ʣ���δϴ�ӣ�ֱ�Ӻ�ɳ�������ʹ���ƫ���������Ƿ�ϴ�������Լ�����������Һ��̼������Һ�ȣ����������غ���Լ����������������������Ӷ��ó���Ԫ�ص���������Ϊ32 m6/233 m1

 С�����ϵ�д�
С�����ϵ�д�