题目内容
【题目】为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,实验过程如下:

请回答:
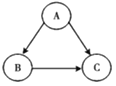
(1)操作①中被磁铁吸引的金属A是_____;金属B是_____。
(2)操作a的名称是_____。
(3)写出步骤②所涉及的化学反应方程式_____,判断步骤②中稀硫酸是否适量依据是:_____。
(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂_____(填标号)。
a.硫酸铜溶液 b.氯化钠溶液 c.硝酸银溶液。
写出有关化学反应方程式_____。
【答案】Fe或铁) Cu(或铜) 过滤 ![]() 根据操作②中不再产生气泡为依据(合理即可) a
根据操作②中不再产生气泡为依据(合理即可) a ![]()
【解析】
(1)铁可以被磁铁吸引,铜和镁不能,操作①中被磁铁吸引的金属A是铁;金属B不能与稀硫酸反应,则金属B是铜;
(2)操作将固体与液体分离,a的名称是:过滤;
(3)步骤②中镁与稀硫酸反应产生硫酸镁和氢气的化学反应方程式:Mg+H2SO4=MgSO4+H2↑,判断步骤②中稀硫酸是否适量依据是:根据操作②中刚好不再产生气泡,则硫酸巧合完全反应;
(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂
a.硫酸铜溶液,镁与硫酸铜反应恰好产生硫酸镁和铜;故选项正确;
b.氯化钠溶液,引入新的杂质;故选项错误;
c.硝酸银溶液,引入新的杂质;故选项错误;故选a。
镁与硫酸铜反应恰好产生硫酸镁和铜的化学方程式:Mg+CuSO4=MgSO4+Cu。

练习册系列答案
相关题目