题目内容
【题目】将暗紫色固体A加热得到固体B和C,同时得到无色气体D。把带火星的木条伸入集气瓶中,木条复燃。把C加入到另一种白色固体E中,混合加热又能得到D,并得白色固体F。
(1)写出下列物质的化学式:A、__________D、_____________E、_____________。
(2)写出加热A的符号表达式:________________;反应基本类型为______________。
(3)实验室收集D的方法有________________理由是_______________(任选一种方法)
【答案】KMnO4 O2 KClO3 KMnO4 ![]() K2MnO4+MnO2+O2 分解反应 向上排空气法 氧气密度比空气大
K2MnO4+MnO2+O2 分解反应 向上排空气法 氧气密度比空气大
【解析】
(1)在D中带火星的木条能复燃,说明D是氧气,暗紫色固体A加热能生成氧气,结合实验室制取氧气的方法和药品的颜色,所以A是高锰酸钾,生成的B和C为锰酸钾或二氧化锰中的一种,把C加入到另一种白色固体E中,混合加热又能得到D氧气,说明C是二氧化锰,B是锰酸钾,E是氯酸钾,生成的白色固体F是氯化钾,推出的各种物质均满足题中的转化关系,推导合理,所以各物质的化学式为:A:KMnO4, D:O2,E:KClO3;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,该反应满足分解反应一变多的条件,所以符号表达式为:KMnO4![]() K2MnO4+MnO2+O2,反应基本类型是:分解反应;
K2MnO4+MnO2+O2,反应基本类型是:分解反应;
(3)在选用气体的收集方法时,一般要考虑气体的溶解性,气体的密度与空气密度的比较,氧气的密度比空气大,可以采用向上排空气法收集氧气.
故答案为:(1)KMnO4;O2;KClO3;
(2)KMnO4 ![]() K2MnO4+MnO2+O2;分解反应;
K2MnO4+MnO2+O2;分解反应;
(3)向上排空气法;氧气密度比空气大。

 53天天练系列答案
53天天练系列答案【题目】某小组对过氧化氢溶液制取氧气进行了如下探究:
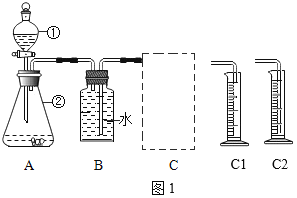
(探究一)探究不同催化剂对H2O2分解速率的影响该小组采用了如图1所示装置进行实验,实验中催化剂均为0.4g,H2O2溶液均为20mL,浓度均为10%。在C框中连接导管和量筒,并测量收集到50mL水时的某项数据,经计算后绘制出下表:
催化剂种类 | 气体产生速率(mL/s) |
二氧化锰 | 3.5 |
氧化铜 | 4.5 |
活性炭 | 5.8 |
(1)检查A装置气密性的方法是:用弹簧夹夹住A装置右侧胶皮管,打开①上方的塞子,向其中加水,打开①的活塞,若_____,则气密性良好。
(2)装置A中发生的反应化学方程式为_____,C框内应选用_____(填“C1”或“C2”)装置。
(3)该探究实验中,需要测定的数据是_____。
(4)从实验数据可知:相同条件下,表中催化剂的催化效果由强到弱依次为_____。
(5)当量筒中收集到50mL水时,H2O2分解产生的氧气体积_____50mL(填“<”、“>”或“=”)。
(探究二)探究MnO2的用量对H2O2分解速率的影响,图2甲所示装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比。反应放热忽略不计)

(1)图2乙是“0.1gMnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出_____。
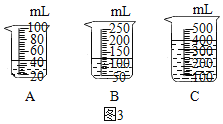
(2)当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线。曲线的斜率显示,当MnO2的用量增加到0.08g时,H2O2的分解速率达到实验要求。在此实验条件下,若MnO2的质量为4g(一药匙)时,能使图3中_____(选填字母)烧杯中所装的3%H2O2溶液中H2O2的分解速率最接近实验要求。
(探究三)探究H2O2溶液的浓度对H2O2分解速率的影响,
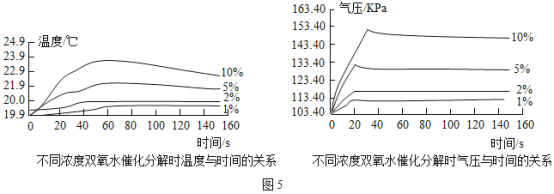
如图4所示,在250mL三颈瓶中均加入0.5gMnO2,在恒压漏斗中各加入20mL不同浓度的H2O2溶液,分别进行实验。用温度传感器测量并绘制出瓶内温度与时间的关系图。如图5①所示。再将该装置的三颈瓶浸入水浴池中(该池可使瓶内的溶液温度恒定在20℃),用上述实验中相同量的各物质重复上述实验,用气压传感器测量并绘制出瓶内气压与时间的关系图,如图5所示。
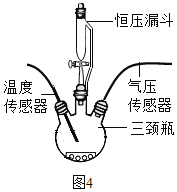
(1)实验中,恒压漏斗的作用是_____。
(2)由图①知道:H2O2分解时会_____热量(填“放出”或“吸收”)。
(3)由图②知道:H2O2溶液浓度越高,H2O2分解速率越_____(填“快”或“慢”)。以10%H2O2溶液为例,约25s后三颈瓶内气压由高缓慢降低的原因是_____。
(反思与总结)影响H2O2分解速率的因素,除了催化剂的种类、催化剂的用量、H2O2溶液的浓度外,还可能有_____
【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
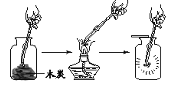
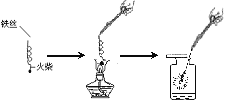
A 木炭燃烧 | B铁丝燃烧 |
(1)木炭在氧气中燃烧时,可观察到的实验现象为______________________。 (2)若验证生成物,需向集气瓶中加入的药品为_________________。 |
(1)铁丝在氧气中燃烧的化学方程式为_______。 (2)实验时,预先在集气瓶里装少量水的作用是_________________________。 |