题目内容
【题目】溶液的微粒构成决定其性质,溶液的宏观组成是其成分计算的依据。
(1)氯化钠晶体是由 (填微粒符号)构成的。氯化钠溶于水,溶液导电能力显著增强,是因为其溶液中含有 ; 氯化钠溶液通电后生成氢氧化钠、氯气和氢气,请写出该化学反应方程式 。
(2)用溶质质量分数为15%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要15%的氯化钠溶液 g,加水 g。
(3)某温度下饱和氯化钠溶液的溶质质量分数为26%,试列式计算该温度下氯化钠的溶解度S(计算结果保留小数点后一位)。
【答案】(1)Na+、Cl-;自由移动的钠离子和氯离子NaCl![]() NaOH +Cl2↑ +H2↑(2)200克;300克(3)35.1克。
NaOH +Cl2↑ +H2↑(2)200克;300克(3)35.1克。
【解析】
试题分析:氯化钠晶体是由Na+、Cl-两种离子构成的。氯化钠溶于水,溶液导电能力显著增强,是因为其溶液中含有自由移动的钠离子和氯离子; 氯化钠溶液通电后生成氢氧化钠、氯气和氢气,该化学反应方程式2NaCl +2H2O![]() 2NaOH +Cl2↑ +H2↑。用溶质质量分数为15%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要15%的氯化钠溶液=500g*6%÷15%=200g,加水的量=500克-200克=300克。设该温度下氯化钠的溶解度S克,则S克/(S克+100克)×100%=26%,则S=35.1克。
2NaOH +Cl2↑ +H2↑。用溶质质量分数为15%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要15%的氯化钠溶液=500g*6%÷15%=200g,加水的量=500克-200克=300克。设该温度下氯化钠的溶解度S克,则S克/(S克+100克)×100%=26%,则S=35.1克。

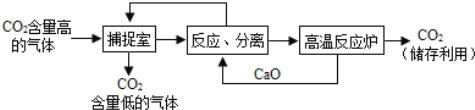
【题目】工业上常利用电石制乙炔气体(C2H2)时产生的灰浆和残渣制备化工原料KClO3和超细CaCO3。
电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:
![]()
其中电石与水反应生成氢氧化钙和乙炔,该反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑ 残渣中主要成分是Ca(OH)2 和CaCO3。
Ⅰ.制备KClO3的流程如下:
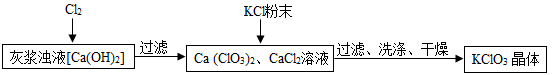
(1)向灰浆浊液中通入Cl2 ,得到Ca(ClO3)2、CaCl2溶液。反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5。写出此反应的化学方程式 。
(2)有关物质在常温下的溶解度如下:
物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
上述流程中加入KCl粉末,KCl与 (填化学式)发生了复分解反应,得到KClO3晶体。你认为能得到KClO3 晶体的原因是 。
(3)洗涤时,可以选用下列 作洗涤剂(填字母编号)。
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):
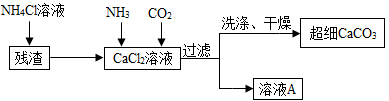
(4)流程中溶液A可循环使用,其主要成分的化学式是 。