题目内容
【题目】某补钙剂(有效成分为碳酸钙。其它成分不含钙元素)的说明中标明含钙量为30%李琳同学为了检验该产品,取10g补钙品放入100g稀盐酸中,![]() 与补钙品有效成分刚好完全反应(其它或分不与盐酸反应)。反应后剩余国体和液体的总质量为107.8g (不包括烧杯的质量,且气体的溶解忽略不计)。
与补钙品有效成分刚好完全反应(其它或分不与盐酸反应)。反应后剩余国体和液体的总质量为107.8g (不包括烧杯的质量,且气体的溶解忽略不计)。
求:(1)补钙品中实际含钙的质量分数是多少?
(2)该补钙剂是否符合说明中的标准?
【答案】(1)20%;(2)该补钙剂不符合符合说明中的标准
【解析】
根据质量守恒定律可得,生成的二氧化碳的质量为10g+100g-107.8g=2.2g
设补钙品中实际含钙的质量分数为x
根据CaCO3+2HCl=CaCl2+H2O+CO2↑可得关系式为

x=20%<30%
答:(1)补钙品中实际含钙的质量分数是20%;(2)该补钙剂不符合符合说明中的标准。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
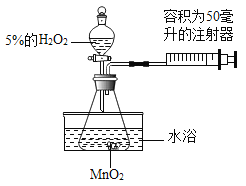
【题目】小金为了探究温度对过氧化氢分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
实验1 | 实验2 | |
二氧化锰的质量/克 | 0.5 | 0.5 |
5%的过氧化氢的体积/毫升 | 40 | 待填 |
水浴温度/℃ | 20 | 80 |
(1)实验2中应加入5%过氧化氢____________毫升;
(2)在两次实验中,可通过_____________________来比较过氧化氢分解反应速率的大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有__________________;