题目内容
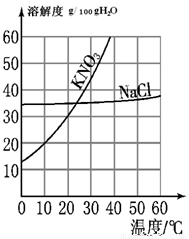
根据如图所示的KNO3和NaCl的溶解度曲线回答下列问题.
①10℃时,KNO3的溶解度约为________g/100g水,若要配制10℃时60g KNO3饱和溶液,需KNO3________g;
②点M表示50℃时,硝酸钾的________溶液(填“饱和”或“不饱和”);
③要从NaCl的饱和溶液中提取NaCl,应采用的方法是________;
A.蒸发结晶 B.降温结晶 C.过滤
④要将硝酸钾的不饱和溶液变成饱和溶液,可采用的方法是________(写出一种).
20 10 不饱和 A 降温或蒸发水或加溶质
分析:①运用溶解度曲线图上某点的意义解答;要配制10℃时60g KNO3饱和溶液,先从图上确定10℃时硝酸钾的溶解度为20g,说明该温度下100g溶剂水中达到饱和状态溶解的硝酸钾的质量为20g,所以50g水中在该温度下最多溶解10g溶质形成60g的硝酸钾的饱和溶液解答.
②运用点M在硝酸钾的溶解度曲线下面,说明溶液中溶解的硝酸钾的质量没达到溶解度故为不饱和溶液解答.
③运用氯化钠的溶解度受温度的影响极小,不能运用降温结晶的方法结晶要选用蒸发结晶法解答.
④运用蒸发溶剂和加溶质都能使不饱和溶液变为饱和溶液,硝酸钾的溶解度随温度升高而增大受温度影响较大降低温度会使硝酸钾的溶解度减小,硝酸钾的不饱和溶液会变成饱和溶液解答.
解答:①10℃时,KNO3的溶解度为20g;要配制10℃时60g KNO3饱和溶液,先从图上确定10℃时硝酸钾的溶解度为20g,说明该温度下100g溶剂水中达到饱和状态溶解的硝酸钾的质量为20g,所以50g水中在该温度下最多溶解10g溶质形成60g的硝酸钾的饱和溶液,故答案:20 10.
②点M在硝酸钾的溶解度曲线下面,说明溶液中溶解的硝酸钾的质量没达到溶解度故为不饱和溶液,故答案不饱和.
③氯化钠的溶解度受温度的影响极小,不能运用降温结晶的方法结晶要选用蒸发结晶法,故答案:A.
④蒸发溶剂和加溶质都能使不饱和溶液变为饱和溶液;硝酸钾的溶解度随温度升高而增大受温度影响较大降低温度会使硝酸钾的溶解度减小,硝酸钾的不饱和溶液会变成饱和溶液,故答案:降温或蒸发水或加溶质.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.
分析:①运用溶解度曲线图上某点的意义解答;要配制10℃时60g KNO3饱和溶液,先从图上确定10℃时硝酸钾的溶解度为20g,说明该温度下100g溶剂水中达到饱和状态溶解的硝酸钾的质量为20g,所以50g水中在该温度下最多溶解10g溶质形成60g的硝酸钾的饱和溶液解答.
②运用点M在硝酸钾的溶解度曲线下面,说明溶液中溶解的硝酸钾的质量没达到溶解度故为不饱和溶液解答.
③运用氯化钠的溶解度受温度的影响极小,不能运用降温结晶的方法结晶要选用蒸发结晶法解答.
④运用蒸发溶剂和加溶质都能使不饱和溶液变为饱和溶液,硝酸钾的溶解度随温度升高而增大受温度影响较大降低温度会使硝酸钾的溶解度减小,硝酸钾的不饱和溶液会变成饱和溶液解答.
解答:①10℃时,KNO3的溶解度为20g;要配制10℃时60g KNO3饱和溶液,先从图上确定10℃时硝酸钾的溶解度为20g,说明该温度下100g溶剂水中达到饱和状态溶解的硝酸钾的质量为20g,所以50g水中在该温度下最多溶解10g溶质形成60g的硝酸钾的饱和溶液,故答案:20 10.
②点M在硝酸钾的溶解度曲线下面,说明溶液中溶解的硝酸钾的质量没达到溶解度故为不饱和溶液,故答案不饱和.
③氯化钠的溶解度受温度的影响极小,不能运用降温结晶的方法结晶要选用蒸发结晶法,故答案:A.
④蒸发溶剂和加溶质都能使不饱和溶液变为饱和溶液;硝酸钾的溶解度随温度升高而增大受温度影响较大降低温度会使硝酸钾的溶解度减小,硝酸钾的不饱和溶液会变成饱和溶液,故答案:降温或蒸发水或加溶质.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.

练习册系列答案
相关题目
 13、根据如图所示的KNO3和NaCl的溶解度曲线回答下列问题.
13、根据如图所示的KNO3和NaCl的溶解度曲线回答下列问题.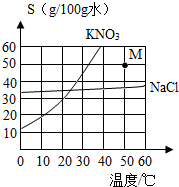
 (2010?崇明县一模)根据如图所示的KNO3和NaCl的溶解度曲线回答下列问题.
(2010?崇明县一模)根据如图所示的KNO3和NaCl的溶解度曲线回答下列问题. 水是非常良好的溶剂,是生活、生产中最重要的物质,请回答下列问题:
水是非常良好的溶剂,是生活、生产中最重要的物质,请回答下列问题: