题目内容
 水是非常良好的溶剂,是生活、生产中最重要的物质,请回答下列问题:
水是非常良好的溶剂,是生活、生产中最重要的物质,请回答下列问题:①KNO3溶于水后得到的溶液,具有稳定性和
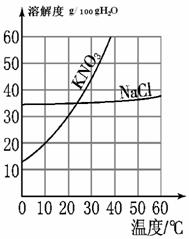
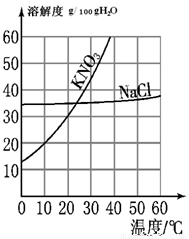
根据如图所示的KNO3和NaCl的溶解度曲线回答下列问题.
②50℃时,KNO3溶解度
③10℃时,KNO3的溶解度约为
④在温度不变的情况下,将NaCl的不饱和溶液变成饱和溶液,可采用恒温蒸发水和
⑤在40℃时,将质量分数相等的KNO3和NaCl溶液,冷却到20℃,此时有关它们质量分数的关系,下列说法错误的是
A.可能KNO3溶液质量分数大
B.可能NaCl溶液质量分数大
C.两者可能仍旧相等.
分析:①溶液具有均一性和稳定性;
②由溶解度曲线图可比较同一温度下不同物质的溶解度大小;
③据溶解度曲线可知某温度下物质的溶解度;
④不饱和溶液变为饱和溶液的一般方法是:增加溶质、蒸发溶剂;
⑤据二者的溶解度随温度变化情况及溶液中溶质的质量分数计算方法分析解答.
②由溶解度曲线图可比较同一温度下不同物质的溶解度大小;
③据溶解度曲线可知某温度下物质的溶解度;
④不饱和溶液变为饱和溶液的一般方法是:增加溶质、蒸发溶剂;
⑤据二者的溶解度随温度变化情况及溶液中溶质的质量分数计算方法分析解答.
解答:解:①溶液具有均一性和稳定性;
②由溶解度曲线图可知:50℃时,KNO3溶解度大于NaCl的溶解度;
③据溶解度曲线可知10℃时,KNO3的溶解度约为:20g或20g/100gH2O;
④在温度不变的情况下,将NaCl的不饱和溶液变成饱和溶液,可采用恒温蒸发水和不加入NaCl的方法;
⑤KNO3的溶解度随温度的降低而降低,NaCl的溶解度随温度变化不大;在40℃时,将质量分数相等的KNO3和NaCl溶液,冷却到20℃,由于降温前溶液不知是否饱和,故降温到20℃时可能二者仍不饱和,则溶质的质量分数不变,也可能二者都达到饱和,据饱和溶液中质量分数的计算式
×100%可知:溶解度大则溶质质量分数大,20℃时氯化钠的溶解度大于硝酸钾的溶解度,所以氯化钠的溶质质量分数大于硝酸钾的溶质质量分数,不可能是A这种情况;
故答案为:①均一;②大于;③20g或20g/100g水;④加入NaCl;⑤A.
②由溶解度曲线图可知:50℃时,KNO3溶解度大于NaCl的溶解度;
③据溶解度曲线可知10℃时,KNO3的溶解度约为:20g或20g/100gH2O;
④在温度不变的情况下,将NaCl的不饱和溶液变成饱和溶液,可采用恒温蒸发水和不加入NaCl的方法;
⑤KNO3的溶解度随温度的降低而降低,NaCl的溶解度随温度变化不大;在40℃时,将质量分数相等的KNO3和NaCl溶液,冷却到20℃,由于降温前溶液不知是否饱和,故降温到20℃时可能二者仍不饱和,则溶质的质量分数不变,也可能二者都达到饱和,据饱和溶液中质量分数的计算式
| 溶解度 |
| 溶解度+100g |
故答案为:①均一;②大于;③20g或20g/100g水;④加入NaCl;⑤A.
点评:本题主要考查了学生对溶液的特征、溶解度曲线的认识、饱和溶液和不饱和溶液的相互转化、溶质的质量分数等知识,能较好考查学生分析、解决问题的能力.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
请参与某学习小组进行研究性学习的过程,并协助完成相关任务:
【提出问题】在平时探讨酸的性质时,我们通常是讨论酸的水溶液.究竟水在酸显示酸的特性时扮演什么角色呢?
【确定研究对象以我们最熟知的盐酸(氯化氢的水溶液)和氯化氢进行探究.
【查阅资料】氯化氢溶于水时解离出氢离子和氯离子,而溶于干燥的甲苯(一种有机溶剂)时仍以氯化氢分子的形式分散(如图1).
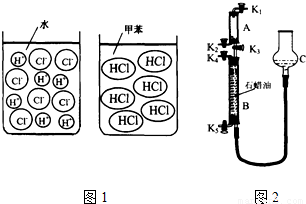
【设计与实验】(请完成下表)
【讨论与反思】盐酸的酸性是因为氯化氢在水分子的作用下解离出了⑤______.
水对酸显现其酸性性质非常重要.还有哪些实例或实验也可以体现水对酸显现其酸性性质的重要性呢,是否没有水,酸就不能显现酸性性质呢?(此问不作答,请在今后的学习中继续关注.)
【拓展探究】该学习小组又尝试用图2所示装置进行氯化氢气体与氨气反应的实验探究,活塞K1、K2、K3、K4、K5均关闭(装置气密性好). 通过调节活塞开关,用排石蜡油的方法在B管中收集满了氨气,如通过调节活塞K1、K2,在干燥的A管中充满与大气压强相等的干燥氯化氢气体,其操作是 ⑥______. 在不用任何试剂的情况下,当看到 ⑦______现象时,说明A管中已收集满了氯化氢气体.打开K3,氯化氢气体与氨气发生化合反应,生成一种铵盐,写出反应的化学方程式:⑧______?
【提出问题】在平时探讨酸的性质时,我们通常是讨论酸的水溶液.究竟水在酸显示酸的特性时扮演什么角色呢?
【确定研究对象以我们最熟知的盐酸(氯化氢的水溶液)和氯化氢进行探究.
【查阅资料】氯化氢溶于水时解离出氢离子和氯离子,而溶于干燥的甲苯(一种有机溶剂)时仍以氯化氢分子的形式分散(如图1).

【设计与实验】(请完成下表)
| 实验内容 | 实验现象 | 解释与结论 |
| 测定导电性 | 氯化氢的水溶液:导电性良好 | 氯化氢的水溶液中有自由移动的离子 |
| 氯化氢的甲苯溶液:不导电 | 氯化氢的甲苯溶液没有自由移动的离子 | |
| 与镁作用 | 氯化氢的水溶液:①______ | 化学方程式: ②______ |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢的甲苯溶液没有解离出氢离子 | |
| 与固态碳酸钠作用 | 氯化氢的水溶液:产生气泡 | 化学方程式: ③______ |
| 氯化氢的甲苯溶液:④______ | 氯化氢的甲苯溶液没有解离出氢离子 |
水对酸显现其酸性性质非常重要.还有哪些实例或实验也可以体现水对酸显现其酸性性质的重要性呢,是否没有水,酸就不能显现酸性性质呢?(此问不作答,请在今后的学习中继续关注.)
【拓展探究】该学习小组又尝试用图2所示装置进行氯化氢气体与氨气反应的实验探究,活塞K1、K2、K3、K4、K5均关闭(装置气密性好). 通过调节活塞开关,用排石蜡油的方法在B管中收集满了氨气,如通过调节活塞K1、K2,在干燥的A管中充满与大气压强相等的干燥氯化氢气体,其操作是 ⑥______. 在不用任何试剂的情况下,当看到 ⑦______现象时,说明A管中已收集满了氯化氢气体.打开K3,氯化氢气体与氨气发生化合反应,生成一种铵盐,写出反应的化学方程式:⑧______?


 约为(13) ;
约为(13) ;