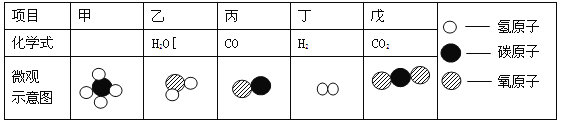
题目内容
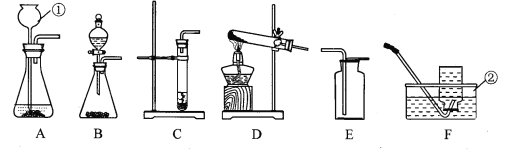
【题目】结合下图所示实验装置回答问题:

(1)指出图中标有数字的仪器名称:① ;② 。
(2)实验室若用高锰酸钾制取氧气,可选用的发生装置是 (填序号),反应的化学方程式为 ;若要收集较为纯净的氧气最好选用 装置(填序号)。实验前还应在试管口放一团棉花,其作用是 ;实验中试管中的棉花没有燃烧,根据燃烧的条件分析,主要原因是 。
(3)实验室用大理石和稀盐酸制取二氧化碳的发生装置应选用 (填序号),反应的化学方程式为 ;若需要控制反应的速率,在装置上可以怎样改进? 。一般不用D装置收集二氧化碳的原因是 。
(4)F装置是一种可用于集气、洗气等的多功能装置。若将F装置内装满水,再连接量筒,就可以用于测定不溶于水且不与水反应的气体体积,则气体应从 (填“a”或“b”)进入F中。
(5)若用F装置检验生成的气体是否是二氧化碳,可先在F装置中加入 ,气体应从 (填“a”或“b”)进入F中。
【答案】(1)酒精灯;集气瓶;
(2)A;2KMnO4![]() K2MnO4+MnO2+O2↑;D;防止固体粉末进入并堵塞导管,导致爆炸;温度没有达到棉花的着火点;
K2MnO4+MnO2+O2↑;D;防止固体粉末进入并堵塞导管,导致爆炸;温度没有达到棉花的着火点;
(3)B;CaCO3+2HCl═CaCl2+CO2↑+H2O;将长颈漏斗换成分液漏斗(或注射器等);二氧化碳能溶于水;
(4)b;
(5)澄清石灰水;a。
【解析】
试题分析:(1)据常用仪器可知标号仪器分别是酒精灯和集气瓶;
(2)高锰酸钾在加热的条件下可以分解产生二氧化锰、锰酸钾和氧气,属于固体加热型,故选发生装置A,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;氧气不易溶于水,所以收集较为纯净的氧气可用排水法;试管口放棉花是为了防止加热时高锰酸钾粉末进入导管;燃烧的条件是可燃物、氧气、达到物质的着火点,前2项已具备,所以棉花未燃烧是因为未达到其着火点;
K2MnO4+MnO2+O2↑;氧气不易溶于水,所以收集较为纯净的氧气可用排水法;试管口放棉花是为了防止加热时高锰酸钾粉末进入导管;燃烧的条件是可燃物、氧气、达到物质的着火点,前2项已具备,所以棉花未燃烧是因为未达到其着火点;
(3)在实验室中制取气体时选择发生装置的依据为药品的状态和反应条件,根据在实验室中制取二氧化碳常用大理石和稀盐酸反应来制取,装置应选择B;化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;若控制反应速率,则须控制反应物的量,可以通过分液漏斗控制液体的流速,从而控制反应的速度;二氧化碳可溶于水,所以不能用排水集气法收集氧气;
(4)气体应从短管b进入,把水从长管a排出,利用量筒盛接的水的体积就是收集的气体的体积;
(5)检验二氧化碳用澄清的石灰水,气体应从长管a进入,与石灰水充分接触而反应。

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析。
【资料1】草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4·3H2O![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是 (填字母编号)。

【资料2】碱石灰是氢氧化钠和氧化钙的混合物,可以吸收水分和二氧化碳;
【资料3】浓硫酸具有吸水性,可以干燥气体;
【资料4】氢氧化钠溶液和石灰水类似都可以与二氧化碳反应,但吸收能力比石灰水强
【问题讨论】用下图所示装置进行实验:
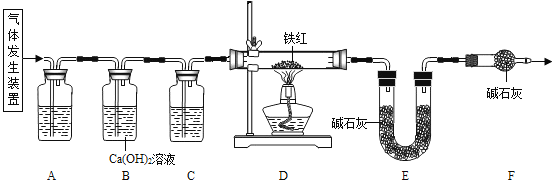
(2)实验前应先 。
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是 (填字母编号)。
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是 。
(5)写出D装置中所发生反应的一个化学方程式 。
【数据分析与计算】
【资料5】铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
(6)称取铁红样品10.0 g,用上述装置进行实验,测定铁红中铁的质量分数。
①D中充分反应后得到Fe粉的质量为m g,则 < m < 。
②待充分反应、冷却后,将D中的固体放入足量的稀硫酸溶液中,产生氢气质量为0.27g,则此铁红样品中铁的质量分数是多少?[写出详细计算过程]
【实验评价】
(7)反思:请指出【问题讨论】中实验装置的一个明显缺陷 。